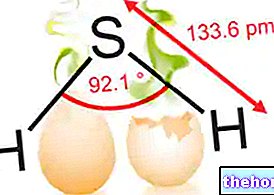
Veikliosios medžiagos: Golimumabas
Simponi 50 mg injekcinis tirpalas užpildytoje švirkštimo priemonėje
Galima įsigyti Simponi pakuotės lapelių dydžių:- Simponi 50 mg injekcinis tirpalas užpildytoje švirkštimo priemonėje
- Simponi 100 mg injekcinis tirpalas užpildytoje švirkštimo priemonėje
Indikacijos Kodėl vartojamas Simponi? Kam tai?
Simponi sudėtyje yra veikliosios medžiagos, vadinamos golimumabu.
Simponi priklauso vaistų, vadinamų TNF blokatoriais, grupei. Jis vartojamas suaugusiesiems gydyti šias uždegimines ligas:
- Reumatoidinis artritas
- Psoriazinis artritas
- Ašinis spondiloartritas, įskaitant ankilozinį spondilitą ir neradiografinį ašinį spondiloartritą
- Opinis kolitas
Vaikams, sveriantiems ne mažiau kaip 40 kg, Simponi vartojamas poliartikuliniam jaunatviniam idiopatiniam artritui gydyti.
Simponi veikia blokuodamas baltymų, vadinamų „naviko nekrozės faktoriumi alfa“ (TNF-α), veikimą. Šis baltymas dalyvauja organizmo uždegiminiuose procesuose ir jį blokuojant galima sumažinti organizmo uždegimą.
Reumatoidinis artritas
Reumatoidinis artritas yra uždegiminė sąnarių liga. Jei sergate aktyviu reumatoidiniu artritu, iš pradžių būsite gydomas kitais vaistais. Jei į šiuos vaistus nepakankamai reaguojate, būsite gydomi Simponi kartu su kitu vaistu, vadinamu metotreksatu:
- Sumažinkite ligos požymius ir simptomus.
- Sulėtinkite kaulų ir sąnarių pažeidimus.
- Pagerinti fizinę funkciją.
Psoriazinis artritas
Psoriazinis artritas yra uždegiminė sąnarių liga, dažniausiai lydima psoriazės, uždegiminės odos ligos. Jei sergate aktyviu psoriaziniu artritu, pirmiausia būsite gydomi kitais vaistais. Jei į šiuos vaistus nebus reaguojama tinkamai, būsite gydomi Simponi skirtas:
- Sumažinkite ligos požymius ir simptomus.
- Sulėtinkite kaulų ir sąnarių pažeidimus.
- Pagerinti fizinę funkciją.
Ankilozuojantis spondilitas ir neradiografinis ašinis spondiloartritas
Ankilozuojantis spondilitas ir neradiografinis ašinis spondiloartritas yra uždegiminės stuburo ligos. Jei sergate ankiloziniu spondilitu ar neradiografiniu ašiniu spondiloartritu, pirmiausia būsite gydomas kitais vaistais. Jei į šiuos vaistus nepakankamai reaguojate, Simponi gydys:
- Sumažinkite ligos požymius ir simptomus.
- Pagerinti fizinę funkciją.
Opinis kolitas
Opinis kolitas yra uždegiminė žarnyno liga. Jei sergate opiniu kolitu, pirmiausia jums bus paskirti kiti vaistai. Jei į šiuos vaistus nepakankamai reaguojate, jums bus skiriamas Simponi jūsų ligai gydyti.
Jaunatvinis idiopatinis poliartritinis artritas
Juvenilinis poliartritinis idiopatinis artritas yra uždegiminė liga, sukelianti vaikų sąnarių skausmą ir patinimą. Jei jūsų vaikas nepakankamai reaguoja į šiuos vaistus, jūsų vaikui bus skiriamas Simponi kartu su metotreksatu.
Kontraindikacijos Kada Simponi vartoti negalima
Simponi vartoti negalima:
- Jeigu yra alergija (padidėjęs jautrumas) golimumabui arba bet kuriai pagalbinei šio vaisto medžiagai (jos išvardytos 6 skyriuje).
- Jei sergate tuberkulioze (TB) ar bet kokia kita rimta infekcija.
- Jei sergate vidutinio sunkumo ar sunkiu širdies nepakankamumu.
Jei nesate tikri, ar kuri nors iš išvardytų būklių Jums tinka, prieš pradėdami vartoti Simponi pasitarkite su gydytoju, vaistininku arba slaugytoju.
Atsargumo priemonės Vartojant prieš vartojant Simponi
Pasitarkite su gydytoju, vaistininku arba slaugytoja, prieš pradėdami vartoti Simponi.
Infekcijos
Nedelsdami pasakykite savo gydytojui, jei gydymo Simponi metu arba po jo jau buvo infekcijos simptomų arba jie atsirado.Infekcijos simptomai yra karščiavimas, kosulys, dusulys, į gripą panašūs simptomai, viduriavimas, žaizdos, dantų problemos ar deginimo pojūtis šlapinantis.
- Vartodami Simponi, galite lengviau užsikrėsti infekcijomis.
- Infekcijos gali progresuoti greičiau ir būti sunkesnės. Be to, praeities infekcijos gali grįžti.
Tuberkuliozė (TB)
Nedelsdami pasakykite gydytojui, jei gydymo metu pastebėjote tuberkuliozės simptomus. TB simptomai yra nuolatinis kosulys, svorio kritimas, nuovargis, karščiavimas ar prakaitavimas naktį.
- Buvo pranešta apie kelis tuberkuliozės atvejus pacientams, gydytiems Simponi, retais atvejais net pacientams, kurie buvo gydomi vaistais nuo tuberkuliozės. Jūsų gydytojas atliks tyrimus, kad nustatytų, ar nesergate tuberkulioze. Šiuos tyrimus gydytojas įrašys į paciento įspėjimo kortelę.
- Labai svarbu pasakyti gydytojui, jei anksčiau sirgote tuberkulioze arba artimai bendravote su asmeniu, kuris serga ar sirgo tuberkulioze.
- Jei gydytojas mano, kad Jums yra tuberkuliozės rizika, prieš Jums skiriant Simponi, galite būti gydomi vaistais nuo tuberkuliozės.
Hepatito B virusas (HBV)
- Prieš skiriant Simponi, pasakykite gydytojui, jei esate nešiotojas arba sirgote ar sirgote hepatitu B.
- Pasakykite gydytojui, jei manote, kad jums gali kilti pavojus užsikrėsti hepatitu B
- Gydytojas turi įvertinti, ar sergate hepatitu B
- Gydymas TNF blokatoriais, tokiais kaip Simponi, gali sukelti hepatito B viruso aktyvavimą pacientams, nešiojantiems šį virusą, o tai kai kuriais atvejais gali sukelti mirtį.
Invazinės grybelinės infekcijos
Nedelsdami pasakykite gydytojui, jei gyvenote ar keliavote į „vietovę, kurioje dažnai atsiranda infekcijų, kurias sukelia tam tikros rūšies grybai, galintys paveikti plaučius ar kitas kūno dalis (vadinamos histoplazmoze, kokcidioidomikoze ar blastomikoze). Paklauskite savo gydytojo, ar jūs nežinote, ar šios grybelinės infekcijos yra dažnos vietovėje, kurioje gyvenote ar keliavote.
Vėžys ir limfoma
Prieš pradėdami vartoti Simponi, pasakykite gydytojui, jei sergate ar kada nors sirgote limfoma (kraujo vėžio rūšimi) ar kitomis vėžio rūšimis.
- Jei vartojate Simponi ar kitus TNF blokatorius, galite padidinti limfomos ar kitos rūšies vėžio riziką.
- Pacientams, sergantiems sunkiu reumatoidiniu artritu ar kitomis uždegiminėmis ligomis, kurie ilgą laiką sirgo šia liga, gali būti didesnė nei vidutinė rizika susirgti limfoma.
- Buvo pranešta apie vėžį, įskaitant neįprastus, kartais mirtinus vėžio atvejus vaikams ir paaugliams, vartojantiems TNF blokuojančių vaistinių preparatų.
- Retais atvejais pacientams, vartojantiems kitus TNF blokatorius, pastebėta specifinė ir sunki limfomos rūšis, vadinama hepatosplenine T-ląstelių limfoma. Dauguma šių pacientų buvo paaugliai arba jauni vyrai. Ši vėžio forma dažniausiai baigiasi mirtimi. Beveik visi šie pacientai taip pat vartojo vaistus, žinomus kaip azatioprinas arba 6-merkaptopurinas. Pasakykite gydytojui, jei kartu su Simponi vartojate azatiopriną arba 6-merkaptopuriną.
- Pacientams, sergantiems sunkia nuolatine astma, lėtine obstrukcine plaučių liga (LOPL) ar rūkantiems, gali padidėti vėžio rizika gydant Simponi. Jei sergate sunkia nuolatine astma, LOPL arba daug rūko, turėtumėte pasitarti su gydytoju, ar gydymas TNF blokatoriais yra tinkamas.
- Kai kuriems golimumabu gydytiems pacientams išsivystė tam tikros odos vėžio rūšys. Jei gydymo metu ar po jo pastebite kokių nors odos išvaizdos pokyčių ar išaugų, pasakykite gydytojui.
Širdies nepakankamumas
Pastebėję naujus ar blogėjančius širdies nepakankamumo simptomus, nedelsdami pasakykite gydytojui. Širdies nepakankamumo simptomai yra dusulys ar pėdų patinimas.
- Buvo pranešta apie stazinio širdies nepakankamumo atsiradimo ar pasunkėjimo atvejus vartojant TNF blokatorius, įskaitant Simponi. Kai kurie iš šių pacientų mirė.
- Jei sergate lengvu širdies nepakankamumu ir esate gydomas Simponi, gydytojas jus atidžiai stebės.
Nervų sistemos liga
Nedelsdami pasakykite gydytojui, jei jums kada nors buvo diagnozuota demielinizuojanti liga, pvz., Išsėtinė sklerozė, arba atsirado tokių simptomų. Simptomai gali būti regėjimo pokyčiai, rankų ir kojų silpnumas, bet kurios kūno dalies tirpimas ar dilgčiojimas. Jūsų gydytojas nuspręs, ar vartoti Simponi.
Dantų operacijos ar procedūros
- Pasakykite gydytojui, jei ketinate atlikti dantų operacijas ar procedūras.
- Pasakykite chirurgui ar odontologui, atliekančiam procedūrą, kad esate gydomas Simponi, parodydami paciento įspėjimo kortelę.
Autoimuninės ligos
Pasakykite gydytojui, jei atsiranda ligos, vadinamos vilklige, simptomai. Simptomai yra nuolatinis bėrimas, karščiavimas, sąnarių skausmas ir nuovargis.
- Retais atvejais žmonėms, gydytiems TNF blokatoriais, atsirado vilkligė.
Kraujo ligos
Kai kuriems pacientams organizmas gali negaminti pakankamai kraujo ląstelių, padedančių organizmui kovoti su infekcijomis arba sustabdyti kraujavimą. Jei karščiuojate nuolat, bet nesuprantate, lengvai atsiranda kraujosruvų ar kraujuojate arba atrodote išblyškęs, nedelsdami kreipkitės į gydytoją. Gydytojas gali nuspręsti nutraukti gydymą.
Jei nesate tikri, ar kuri nors iš išvardytų būklių Jums tinka, prieš pradėdami vartoti Simponi pasitarkite su gydytoju arba vaistininku.
Vakcinos
Pasakykite gydytojui, jei neseniai buvote paskiepytas arba planuojate skiepytis.
- Gydydamiesi Simponi, neturite gauti tam tikrų (gyvų) vakcinų.
- Kai kurios vakcinacijos gali sukelti infekciją. Jei Simponi vartojote būdama nėščia, jūsų kūdikiui gali padidėti rizika susirgti šia infekcija maždaug šešis mėnesius po paskutinės nėštumo metu gautos dozės. Svarbu pasakyti savo pediatrui ir kitiems sveikatos priežiūros specialistams apie Simponi vartojimą. gali nuspręsti, kada vaikui skiepytis.
Pasitarkite su savo vaiko gydytoju dėl jūsų vaiko skiepų. Jei įmanoma, prieš pradėdami vartoti Simponi, jūsų vaikas turi būti informuotas apie visas vakcinacijas.
Infekcinės terapinės priemonės
Pasitarkite su gydytoju, jei neseniai vartojote ar planuojate gydyti infekcinę terapinę priemonę (pvz., BCG lašinimą, naudojamą vėžiui gydyti).
Alerginės reakcijos
Nedelsdami pasakykite gydytojui, jei po gydymo Simponi atsiranda alerginės reakcijos simptomų. Alerginės reakcijos simptomai gali būti veido, lūpų, burnos ar gerklės patinimas, dėl kurio gali pasunkėti rijimas ar kvėpavimas, odos bėrimas, dilgėlinė, rankų, pėdų ir kulkšnių patinimas.
- Kai kurios iš šių reakcijų gali būti sunkios arba retai pavojingos gyvybei.
- Kai kurios iš šių reakcijų atsiranda po pirmojo Simponi vartojimo.
Vaikai ir paaugliai
Simponi nerekomenduojama vaikams, sveriantiems mažiau nei 40 kg, sergantiems poliartritiniu jaunatviniu idiopatiniu artritu, arba vaikams ir paaugliams iki 18 metų dėl kitų ligų.
Sąveika Kurie vaistai ar maistas gali pakeisti Simponi poveikį
- Pasakykite gydytojui arba vaistininkui, jei vartojate, neseniai vartojote arba galite vartoti kitų vaistų, įskaitant bet kokius kitus vaistus, skirtus reumatoidiniam artritui, poliartritiniam jaunatviniam idiopatiniam artritui, psoriaziniam artritui, ankiloziniam spondilitui, ašiniam spondiloartritui, ne radiografiniam ar opiniam kolitui gydyti.
- Simponi negalima vartoti su vaistais, kurių sudėtyje yra veikliosios medžiagos anakinros arba abatacepto. Šie vaistai naudojami reumatinėms ligoms gydyti.
- Pasakykite gydytojui arba vaistininkui, jei vartojate kokių nors kitų imuninę sistemą veikiančių vaistų.
- Vartojant Simponi, jo negalima gydyti tam tikromis (gyvomis) vakcinomis.
Jei nesate tikri, ar kuri nors iš išvardytų būklių Jums tinka, prieš pradėdami vartoti Simponi pasitarkite su gydytoju arba vaistininku.
Įspėjimai Svarbu žinoti, kad:
Nėštumas ir žindymo laikotarpis
Pasitarkite su gydytoju, prieš pradėdami vartoti Simponi, jei:
- Vartodama Simponi esate nėščia arba planuojate pastoti. Šio vaisto poveikis nėščioms moterims nežinomas. Simponi vartoti nėščioms moterims nerekomenduojama. Jei planuojate gydytis Simponi, gydymo metu ir mažiausiai 6 mėnesius po paskutinės Simponi injekcijos turėtumėte vengti pastoti, naudodami tinkamas kontracepcijos priemones.
- Prieš žindymą paskutinis gydymas Simponi turi būti atliktas mažiausiai prieš 6 mėnesius.
- Jei Simponi vartojote nėštumo metu, jūsų kūdikiui gali būti didesnė infekcijos rizika.Prieš pradedant skiepyti vaiką, svarbu pasakyti pediatrui ir kitiems sveikatos priežiūros specialistams apie Simponi vartojimą (daugiau informacijos rasite skiepų skyriuje).
Jeigu esate nėščia, žindote kūdikį, manote, kad galbūt esate nėščia arba planuojate pastoti, tai prieš vartodama šį vaistą pasitarkite su gydytoju arba vaistininku.
Vairavimas ir mechanizmų valdymas
Simponi gali šiek tiek sutrikdyti jūsų gebėjimą vairuoti ir valdyti įrankius ar mechanizmus. Vartodami Simponi galite svaigti galva. Tokiu atveju nevairuokite ir nevaldykite jokių įrankių ar mechanizmų.
Simponi sudėtyje yra latekso ir sorbitolio
Jautrumas lateksui
Jautrumas lateksui Vienoje užpildyto švirkštimo priemonės dalyje, adatos dangtelyje, yra latekso Kadangi lateksas gali sukelti sunkias alergines reakcijas, prieš pradėdami vartoti Simponi pasakykite gydytojui, jei jūs ar jūsų globėjas esate alergiškas lateksui.
Sorbitolio netoleravimas
Simponi sudėtyje yra sorbitolio (E420). Jei gydytojas Jums yra sakęs, kad netoleruojate kokių nors angliavandenių, prieš vartodami šį vaistą pasitarkite su gydytoju.
Dozavimas ir vartojimo metodas Kaip vartoti Simponi: Dozavimas
Visada vartokite šį vaistą tiksliai kaip nurodė gydytojas arba vaistininkas. Jei abejojate, turėtumėte pasitarti su gydytoju arba vaistininku.
Kiek skiriama Simponi
Reumatoidinis artritas, psoriazinis artritas ir ašinis spondiloartritas, įskaitant ankilozuojantį spondilitą ir neradiografinį ašinį spondiloartritą:
- Rekomenduojama dozė yra 50 mg (1 užpildytos švirkštimo priemonės turinys), vartojama kartą per mėnesį, tą pačią mėnesio dieną.
- Pasitarkite su gydytoju prieš pradėdami vartoti ketvirtąją dozę. Jūsų gydytojas nuspręs, ar tęsti gydymą Simponi.
- Jei sveriate daugiau nei 100 kg, dozę galima padidinti iki 100 mg (2 užpildytų švirkštimo priemonių), suleidžiamos vieną kartą per mėnesį, visada tą pačią mėnesio dieną.
Jaunatvinis idiopatinis poliartritas:
- Rekomenduojama dozė yra 50 mg vieną kartą per mėnesį, tą pačią mėnesio dieną.
- Pasitarkite su savo vaiko gydytoju, prieš pradėdami vartoti ketvirtąją dozę. Jūsų vaiko gydytojas nuspręs, ar tęsti gydymą Simponi.
Opinis kolitas
- Žemiau esančioje lentelėje parodyta, kaip paprastai naudosite šį vaistą.
- Pacientams, sveriantiems mažiau nei 80 kg, 50 mg (1 užpildytos švirkštimo priemonės turinys) praėjus 4 savaitėms po paskutinio gydymo, vėliau-kas 4 savaites.
- Pacientams, sveriantiems 80 kg ar daugiau, 100 mg (2 užpildytų švirkštimo priemonių turinys) praėjus 4 savaitėms po paskutinio gydymo, vėliau-kas 4 savaites.
Kaip duodamas Simponi
- Simponi švirkščiamas po oda (po oda).
- Iš pradžių jūsų gydytojas ar slaugos personalas švirkščia Simponi, tačiau jūs ir jūsų gydytojas gali nuspręsti, kad galite patys susišvirkšti Simponi. Tokiu atveju jums bus nurodyta, kaip patiems susišvirkšti Simponi.
Pasitarkite su gydytoju, jei turite kokių nors klausimų apie injekciją. Šio lapelio pabaigoje rasite išsamią „Vartojimo instrukciją“.
Pamiršus pavartoti Simponi
Jei pamiršote pavartoti Simponi numatytą dieną, suleiskite praleistą dozę, kai tik prisiminsite.
Negalima vartoti dvigubos dozės norint kompensuoti praleistą dozę.
Kada švirkšti kitą dozę:
- Jei pavėlavote mažiau nei 2 savaites, suleiskite praleistą dozę, kai tik prisiminsite, ir toliau laikykitės pradinės schemos.
- Jei pavėlavote daugiau nei 2 savaites, suleiskite pamirštą dozę, kai tik prisiminsite, pasakykite gydytojui arba vaistininkui ir paklauskite, kada vartoti kitą dozę.
Jei nežinote, ką daryti, kreipkitės į gydytoją, vaistininką arba slaugytoją.
Nustojus vartoti Simponi
Jei ketinate nutraukti Simponi vartojimą, pirmiausia pasitarkite su gydytoju arba vaistininku.
Jeigu kiltų daugiau klausimų dėl šio vaisto vartojimo, kreipkitės į gydytoją arba vaistininką.
Perdozavimas Ką daryti pavartojus per didelę Simponi dozę
Jei pavartojote arba suleidote per daug Simponi (suleidote per daug vienkartine doze arba vartojote per daznai), nedelsdami pasakykite gydytojui arba vaistininkui Visada su savimi pasiimkite išorine kartonine pakuote ir šį lapeli, net jei jis tuščias.
Šalutinis poveikis Koks yra Simponi šalutinis poveikis
Šis vaistas, kaip ir visi kiti, gali sukelti šalutinį poveikį, nors jis pasireiškia ne visiems žmonėms. Kai kuriems pacientams gali pasireikšti sunkus šalutinis poveikis, dėl kurio gali prireikti medicininio gydymo. Kai kurių šalutinių poveikių rizika yra didesnė vartojant 100 mg dozę, palyginti su 50 mg doze. Nepageidaujamas poveikis taip pat gali pasireikšti praėjus keliems mėnesiams po paskutinės injekcijos.
Nedelsdami pasakykite gydytojui, jei pastebėjote bet kurį iš šių sunkių Simponi šalutinių poveikių, įskaitant:
- alerginės reakcijos, kurios gali būti sunkios arba retai pavojingos gyvybei (retos). Alerginės reakcijos simptomai gali būti veido, lūpų, burnos ar gerklės patinimas, dėl kurio gali pasunkėti rijimas ar kvėpavimas, odos bėrimas, dilgėlinė, rankų, pėdų ar kulkšnių patinimas. Kai kurios iš šių reakcijų pasireiškė po pirmojo Simponi vartojimo.
- sunkios infekcijos (įskaitant tuberkuliozę, bakterines infekcijas, įskaitant sunkias kraujo infekcijas ir pneumoniją, sunkias grybelines infekcijas ir kitas oportunistines infekcijas) (dažnas). Infekcijos simptomai gali būti karščiavimas, nuovargis, (nuolatinis) kosulys, dusulys, į gripą panašūs simptomai, svorio kritimas, prakaitavimas naktį, viduriavimas, žaizdos, dantų problemos ir deginimo pojūtis šlapinantis.
- hepatito B viruso suaktyvinimas, jei esate nešiotojas arba anksčiau sirgote hepatitu B (retai). Simptomai gali būti odos ir akių pageltimas, tamsiai rudas šlapimas, skausmas dešinėje pilvo pusėje, karščiavimas, bloga savijauta, negalavimas ir labai pavargęs.
- nervų sistemos liga, tokia kaip išsėtinė sklerozė (reta). Nervų sistemos ligos simptomai gali būti regėjimo pokyčiai, rankų ar kojų silpnumas, bet kurios kūno dalies tirpimas ar dilgčiojimas.
- limfmazgių vėžys (limfoma) (retas). Limfomos simptomai gali būti patinę limfmazgiai, svorio kritimas ar karščiavimas.
- širdies nepakankamumas (retas). Širdies nepakankamumo simptomai gali būti dusulys ar pėdų patinimas.
- imuninės sistemos sutrikimų požymiai: - vilkligė (reta). Simptomai gali būti sąnarių skausmas ar bėrimas ant skruostų ar rankų, jautrus saulei. - sarkoidozė (reta). Simptomai gali būti nuolatinis kosulys, dusulys, krūtinės skausmas, karščiavimas, padidėję limfmazgiai, svorio kritimas, bėrimas ir neryškus matymas.
- smulkių kraujagyslių patinimas (vaskulitas) (retas). Simptomai gali būti karščiavimas, galvos skausmas, svorio kritimas, prakaitavimas naktį, bėrimas ir nervų problemos, tokios kaip tirpimas ir dilgčiojimas.
- odos vėžys (nedažnas). Odos vėžio simptomai gali apimti odos išvaizdos pokyčius ar odos išaugimą.
- kraujo liga (dažna). Kraujo ligos simptomai gali būti karščiavimas, kuris nepraeina, stiprus polinkis į mėlynes ar kraujavimą arba labai blyški išvaizda.
- kraujo vėžys (leukemija) (retas). Leukemijos simptomai gali būti karščiavimas, nuovargis, dažnos infekcijos, mėlynės ir prakaitavimas naktį.
Pastebėję bet kurį iš aukščiau išvardytų simptomų, nedelsdami pasakykite gydytojui.
Vartojant Simponi, pastebėtas toks papildomas šalutinis poveikis:
Labai dažnas šalutinis poveikis (gali pasireikšti daugiau kaip 1 iš 10 žmonių):
- Viršutinių kvėpavimo takų infekcijos, gerklės skausmas ar užkimimas, šaltis
Dažnas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 10 žmonių):
- Nenormalūs kepenų tyrimai (padidėjęs kepenų fermentų kiekis), nustatomi atliekant kraujo tyrimus, kuriuos atliko gydytojas
- Galvos svaigimas
- Galvos skausmas
- Jausmas ar dilgčiojimas
- Paviršinės grybelinės infekcijos
- Pūlinys
- Bakterinės infekcijos (pvz., Celiulitas)
- Raudonųjų kraujo kūnelių sumažėjimas
- Teigiamas kraujo tyrimas dėl vilkligės
- Alerginės reakcijos
- Nevirškinimas
- Skrandžio skausmas
- Pykinimas
- Įtaka
- Bronchitas
- Sinusinė infekcija
- Veido pūslelinė
- Aukštas kraujo spaudimas
- Karščiavimas
- Astma, dusulys, švokštimas
- Skrandžio ir žarnyno sutrikimai, įskaitant skrandžio ir storosios žarnos uždegimą, kuris gali sukelti karščiavimą
- Skausmas ir opos burnoje
- Reakcijos injekcijos vietoje (įskaitant paraudimą, kietumą, skausmą, kraujosruvas, niežėjimą, dilgčiojimą ir dirginimą)
- Plaukų slinkimas
- Bėrimas ir odos niežėjimas
- Sunku užmigti
- Depresija
- Silpnumo jausmas
- Kaulų lūžiai
- Krūtinės skausmas
Nedažnas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių):
- Inkstų infekcija
- Vėžys, įskaitant odos vėžį ir nevėžinius gabalėlius ar mažas mases, įskaitant apgamus
- Odos pūslės
- Psoriazė (įskaitant delnų ir (arba) padų ir (arba) odos pustulių formą)
- Trombocitų kiekio sumažėjimas
- Baltųjų kraujo ląstelių kiekio sumažėjimas
- Kombinuotas trombocitų, raudonųjų ir baltųjų kraujo kūnelių sumažėjimas
- Skydliaukės sutrikimai
- Padidėjęs cukraus kiekis kraujyje
- Padidėjęs cholesterolio kiekis kraujyje
- Pusiausvyros sutrikimai
- Regos sutrikimai
- Nereguliaraus širdies plakimo jausmas
- Širdies kraujagyslių susiaurėjimas
- Kraujo krešuliai
- Paraudimas
- Vidurių užkietėjimas
- Lėtinis plaučių uždegimas
- Rūgšties refliuksas
- Akmenys tulžyje
- Kepenų problemos
- Krūties sutrikimai
- Menstruacijų sutrikimai
Retas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 1000 žmonių):
- Kaulų čiulpų nesugebėjimas gaminti kraujo ląstelių
- Sąnarių ar aplinkinių audinių infekcija
- Sunkus gijimas
- Vidaus organų kraujagyslių uždegimas
- Leukemija
- Melanoma (odos vėžio rūšis)
- Odos lupimasis
- Imunologiniai sutrikimai, galintys paveikti plaučius, odą ir limfmazgius (labai dažnai pasireiškia kaip sarkoidozė)
- Pirštų ar kojų pirštų skausmas ir spalvos pasikeitimas
- Skonio sutrikimai
- Šlapimo pūslės sutrikimai
- Inkstų problemos
- Odos kraujagyslių uždegimas, sukeliantis bėrimą
Šalutinis poveikis, kurio dažnis nežinomas:
- Merkelio ląstelių karcinoma (odos vėžio rūšis)
- Retas kraujo vėžys, kuris dažniausiai pasireiškia jauniems žmonėms (hepatospleninė T-ląstelių limfoma)
Pranešimas apie šalutinį poveikį
Jeigu pasireiškė šalutinis poveikis (net jeigu jis šiame lapelyje nenurodytas), kreipkitės į gydytoją, vaistininką arba slaugytoją. Apie šalutinį poveikį taip pat galite pranešti tiesiogiai naudodamiesi V priede nurodyta nacionaline pranešimo sistema. suteikti daugiau informacijos apie šio vaisto saugumą.
Galiojimo laikas ir išlaikymas
- Šį vaistą laikykite vaikams nepastebimoje ir nepasiekiamoje vietoje.
- Ant etiketės ir dėžutės po „Tinka iki“ nurodytam tinkamumo laikui pasibaigus, šio vaisto vartoti negalima. Vaistas tinkamas vartoti iki paskutinės nurodyto mėnesio dienos.
- Laikyti šaldytuve (2 ° C-8 ° C). Negalima užšaldyti.
- Užpildytą švirkštimo priemonę laikykite išorinėje dėžutėje, kad vaistas būtų apsaugotas nuo šviesos.
- Nevartokite šio vaisto, jei pastebėjote, kad skystis nėra nuo šviesiai iki šviesiai geltonos spalvos, drumstas arba jame yra pašalinių dalelių.
- Neišmeskite jokių vaistų į kanalizaciją ar buitines atliekas. Paklauskite savo gydytojo ar vaistininko, kaip išmesti nebenaudojamus vaistus. Tai padės apsaugoti aplinką.
Kita informacija
Simponi sudėtis
Veiklioji medžiaga yra golimumabas. Vienoje 0,5 ml užpildytoje švirkštimo priemonėje yra 50 mg golimumabo.
Pagalbinės medžiagos yra sorbitolis (E420), L-histidinas, L-histidino monohidrochlorido monohidratas, polisorbatas 80 ir injekcinis vanduo.
Simponi išvaizda ir kiekis pakuotėje
Simponi tiekiamas kaip injekcinis tirpalas vienkartinėje užpildytoje švirkštimo priemonėje. Simponi tiekiamas pakuotėmis, kuriose yra 1 užpildytas švirkštiklis, ir daugybinėse pakuotėse, kuriose yra 3 užpildytos švirkštimo priemonės (3 pakuotės po 1). Gali būti tiekiamos ne visų dydžių pakuotės.
Tirpalas yra skaidrus arba šiek tiek opalescuojantis (blizgantis kaip perlas), bespalvis arba šviesiai geltonas ir gali turėti smulkių permatomų arba baltų baltymų dalelių. Nenaudokite Simponi, jei tirpalas pakeitė spalvą, buvo drumstas arba jame yra matomų pašalinių dalelių.
Šaltinio pakuotės lapelis: AIFA (Italijos vaistų agentūra). Turinys paskelbtas 2016 m. Sausio mėn. Pateikta informacija gali būti neatnaujinta.
Norint pasiekti naujausią versiją, patartina apsilankyti AIFA (Italijos vaistų agentūra) svetainėje. Atsisakymas ir naudinga informacija.
01.0 VAISTINIO PREPARATO PAVADINIMAS
SIMPONI 50 MG INJEKTAVIMAS
02.0 KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
Simponi 50 mg injekcinis tirpalas užpildytoje švirkštimo priemonėje
Vienoje 0,5 ml užpildytoje švirkštimo priemonėje yra 50 mg golimumabo *.
Simponi 50 mg injekcinis tirpalas užpildytame švirkšte
Viename 0,5 ml užpildytame švirkšte yra 50 mg golimumabo *.
* IgG1 žmogaus monokloninis antikūnas? pagamintas iš pelių hibridomos ląstelių linijos, naudojant rekombinantinę DNR technologiją.
Pagalbinė medžiaga, kurios poveikis žinomas:
Kiekvienoje užpildytoje švirkštimo priemonėje yra: 20,5 mg sorbitolio 50 mg dozei.
Kiekviename užpildytame švirkšte yra: 20,5 mg sorbitolio 50 mg dozei.
Išsamų pagalbinių medžiagų sąrašą žr. 6.1 skyriuje.
03.0 FARMACINĖ FORMA
Injekcinis tirpalas užpildytoje švirkštimo priemonėje (injekcija), „SmartJect“
Injekcinis tirpalas užpildytame švirkšte (injekcija)
Tirpalas yra skaidrus arba šiek tiek opalescuojantis, bespalvis arba šviesiai gelsvas.
04.0 KLINIKINĖ INFORMACIJA
04.1 Terapinės indikacijos
Reumatoidinis artritas (RA)
Simponi kartu su metotreksatu (MTX) yra skirtas:
• vidutinio sunkumo ir sunkaus aktyvaus reumatoidinio artrito gydymas suaugusiems pacientams, kai nepakankamai reaguojama į ligas modifikuojančius vaistus nuo reumato (DMARD), įskaitant MTX.
• sunkaus, aktyvaus ir progresuojančio reumatoidinio artrito gydymas suaugusiems, kurie anksčiau nebuvo gydomi MTX.
Įrodyta, kad Simponi kartu su MTX sumažina sąnarių pažeidimo progresavimo greitį, matuojamą rentgeno spinduliais, ir pagerina fizinę funkciją.
Nepilnamečių idiopatinis artritas
Jaunatvinis idiopatinis poliartritas (PIA)
Simponi kartu su MTX skirtas poliartritiniam jaunatviniam idiopatiniam artritui gydyti vaikams, sveriantiems ne mažiau kaip 40 kg, kurie nepakankamai reagavo į ankstesnį gydymą MTX.
Psoriazinis artritas (AP)
Simponi, vartojamas atskirai arba kartu su metotreksatu (MTX), skirtas aktyviam ir progresuojančiam psoriaziniam artritui gydyti suaugusiesiems, kai atsakas į ankstesnį gydymą DMARD buvo nepakankamas. Įrodyta, kad Simponi mažina vaisto progresavimo greitį. periferinių sąnarių pažeidimas, matuojamas rentgeno spinduliais pacientams, sergantiems simetriškais poliartikulinių ligų potipiais (žr. 5.1 skyrių), ir pagerinti fizinę funkciją.
Ašinis spondiloartritas
Ankilozuojantis spondilitas (AS)
Simponi skirtas sunkiam, aktyviam ankiloziniam spondilitui gydyti suaugusiesiems, kurie nepakankamai reagavo į įprastą gydymą.
Neradiografinis ašinis spondiloartritas (ašinis SpA nr)
Simponi skirtas suaugusiems pacientams, sergantiems sunkiu aktyviu neradiografiniu ašiniu spondiloartritu, turinčiu objektyvių uždegimo požymių, kaip rodo padidėjęs C reaktyvusis baltymas (CRP) ir (arba) magnetinio rezonanso tomografija (MRT), gydyti suaugusiems pacientams, kurių atsakas buvo nepakankamas. arba netoleruoja nesteroidinių vaistų nuo uždegimo (NVNU).
Opinis kolitas (CU)
Simponi skiriamas vidutinio sunkumo ir sunkaus opinio kolito gydymui suaugusiems pacientams, kurie nepakankamai reagavo į įprastą gydymą, įskaitant kortikosteroidus ir 6-merkaptopuriną (6-MP) arba azatiopriną (AZA), arba kurie netoleruoja arba kuriems yra medicininė kontraindikacija šiems gydymo būdams.
04.2 Dozavimas ir vartojimo metodas
Gydymą Simponi turi pradėti ir prižiūrėti gydytojas specialistas, turintis reumatoidinio artrito, poliartikulinio jaunatvinio idiopatinio artrito, psoriazinio artrito, ankilozinio spondilito, neradiografinio ašinio spondiloartrito ar opinio kolito diagnozavimo ir gydymo patirties. Simponi gydomiems pacientams turi būti įspėtas pacientas. Kortelė.
Dozavimas
Reumatoidinis artritas
Simponi 50 mg skiriamas kartą per mėnesį, tą pačią mėnesio dieną.
Simponi turi būti skiriamas kartu su MTX.
Psoriazinis artritas, ankilozuojantis spondilitas arba neradiografinis ašinis spondiloartritas
Simponi 50 mg skiriamas kartą per mėnesį, tą pačią mėnesio dieną.
Esant visoms aukščiau išvardytoms indikacijoms, turimi duomenys rodo, kad klinikinis atsakas paprastai pasiekiamas per 12–14 savaičių nuo gydymo pradžios (po 3–4 dozių). Reikia apsvarstyti galimybę tęsti gydymą pacientams, kurie neparodo terapinės naudos per šį laiką.
Pacientai, kurių kūno svoris didesnis nei 100 kg
Visoms aukščiau išvardytoms indikacijoms, pacientams, sergantiems RA, AP, SA ar ašiniu SpA nr, sveriančiais daugiau nei 100 kg, kurie nepasiekia tinkamo klinikinio atsako po 3 ar 4 dozių, golimumabo dozę reikia padidinti iki 100 mg kartą per mėnesį, atsižvelgiant į padidėjusią kai kurių sunkių nepageidaujamų reakcijų riziką vartojant 100 mg dozę, palyginti su 50 mg doze (žr. 4.8 skyrių). Reikia apsvarstyti galimybę tęsti gydymą pacientams, kuriems po 3- 4 papildomos 100 mg dozės.
Opinis kolitas
Pacientai, kurių kūno svoris yra mažesnis nei 80 kg
Simponi skiriama kaip pradinė 200 mg dozė, po to 100 mg 2 savaitę, po to po 50 mg kas 4 savaites (žr. 5.1 skyrių).
Pacientai, kurių kūno svoris yra didesnis arba lygus 80 kg
Simponi skiriama kaip pradinė 200 mg dozė, po to 100 mg 2 savaitę, po to po 100 mg kas 4 savaites (žr. 5.1 skyrių).
Palaikomojo gydymo metu kortikosteroidų gali būti palaipsniui mažinama pagal klinikinės praktikos gaires.
Turimi duomenys rodo, kad klinikinis atsakas paprastai pasiekiamas per 12–14 gydymo savaičių (po 4 dozių). Reikėtų apsvarstyti galimybę tęsti gydymą pacientams, kurie per šį laikotarpį neparodo terapinės naudos.
Praleista dozė
Jei pacientas pamiršo suleisti Simponi numatytą dieną, praleistą dozę reikia sušvirkšti, kai tik pacientas prisimena. Pacientus reikia informuoti, kad negalima švirkšti dvigubos dozės norint kompensuoti praleistą dozę.
Kita dozė turi būti skiriama pagal šią instrukciją:
• Jei vėluojama dozė yra trumpesnė nei 2 savaitės, pacientas turi suleisti praleistą dozę ir toliau laikytis pradinės schemos.
• Jei atidėtas dozavimas yra ilgesnis nei 2 savaitės, pacientas turi suleisti praleistą dozę ir nuo šios injekcijos datos reikės nustatyti naują dozavimo schemą.
Specialios populiacijos
Senyvo amžiaus (≥ 65 metų)
Senyviems žmonėms dozės koreguoti nereikia.
Inkstų ir kepenų funkcijos sutrikimas
Šių pacientų populiacijose Simponi netirtas. Dozavimo rekomendacijų pateikti negalima.
Vaikų populiacija
Simponi saugumas ir veiksmingumas jaunesniems nei 18 metų pacientams, sergantiems kitomis indikacijomis nei PV, nenustatytas.
Jaunatvinis idiopatinis poliartritinis artritas
Simponi 50 mg kartą per mėnesį, tą pačią kiekvieno mėnesio dieną, vaikams, kurių kūno svoris ne mažesnis kaip 40 kg.
Turimi duomenys rodo, kad klinikinis atsakas paprastai pasiekiamas per 12–14 gydymo savaičių (po 3–4 dozių). Vaikams, kurie per šį laikotarpį neparodo terapinės naudos įrodymų, reikia tęsti gydymą.
Vartojimo metodas
Simponi skirtas vartoti po oda. Po tinkamo poodinės injekcijos technikos apmokymo pacientai galės savarankiškai susišvirkšti Simponi, jei gydytojas nustatys, kad gali, ir prireikus tinkamai prižiūri. Pacientams reikia nurodyti, kad reikia sušvirkšti visą Simponi kiekį pagal visas vartojimo instrukcijas, pateiktas pakuotės lapelyje.Jei reikia kelių injekcijų, injekcijos turi būti atliekamos skirtingose kūno vietose.
Vartojimo instrukcijas žr. 6.6 skyriuje.
04.3 Kontraindikacijos
Padidėjęs jautrumas veikliajai arba bet kuriai 6.1 skyriuje nurodytai pagalbinei medžiagai.
Aktyvi tuberkuliozė (TB) ar kitos sunkios infekcijos, tokios kaip sepsis ir oportunistinės infekcijos (žr. 4.4 skyrių).
Pacientai, kuriems yra vidutinio sunkumo ar sunkus širdies nepakankamumas (NYHA - Niujorko širdies asociacijos III / IV klasė) (žr. 4.4 skyrių).
04.4 Specialūs įspėjimai ir tinkamos atsargumo priemonės
Infekcijos
Prieš gydymą Simponi, jo metu ir po jo pacientus reikia atidžiai stebėti dėl infekcijų, įskaitant tuberkuliozę. Kadangi golimumabo eliminacija gali užtrukti iki 5 mėnesių, šį laikotarpį reikia tęsti stebėjimą. Jei pacientui pasireiškia sunkios infekcijos ar sepsis, Simponi toliau gydyti negalima (žr. 4.3 skyrių).
Simponi negalima vartoti pacientams, kuriems yra kliniškai reikšminga, aktyvi infekcija. Svarstant apie Simponi vartojimą pacientams, sergantiems lėtine infekcija arba pasikartojančioms infekcijoms, reikia būti atsargiems. Pacientus reikia tinkamai informuoti apie būtinybę vengti galimų infekcijų rizikos veiksnių poveikio.
Pacientai, vartojantys TNF blokuojančius vaistus, yra labiau linkę į sunkias infekcijas.
Pacientams, gydytiems Simponi, buvo pranešta apie bakterines infekcijas (įskaitant sepsį ir pneumoniją), mikobakterijas (įskaitant tuberkuliozę), invazines grybelines infekcijas ir oportunistines infekcijas, įskaitant mirtinas. Kai kurios iš šių sunkių infekcijų išsivystė pacientams, kurie tuo pat metu gydomi imunosupresantais, kurie, be pagrindinės ligos, gali paskatinti juos užsikrėsti. Pacientus, kuriems Simponi gydymo metu atsiranda nauja infekcija, reikia atidžiai stebėti ir atlikti „kruopštų diagnostinį įvertinimą. Simponi vartojimą reikia nutraukti, jei pacientui pasireiškia nauja sunki infekcija ar sepsis ir tinkamai pradedamas“ gydymas. Pacientams, kurie gyveno regionuose ar į juos keliavo, kur invazinės grybelinės infekcijos, tokios kaip histoplazmozė, kokcidioidomikozė ar blastomikozė, yra endeminės, gydymo Simponi nauda ir rizika turi būti atidžiai apsvarstyta. prieš pradedant gydymą Simponi. Didelės rizikos pacientams, gydomiems Simponi, invazinė grybelinė infekcija, turėtų būti įtariama, jei jiems išsivysto sunki sisteminė liga. Jei įmanoma, šiems pacientams empirinis priešgrybelinis gydymas turi būti diagnozuotas ir skiriamas pasitarus su gydytoju, turinčiu patirties gydant pacientus, sergančius invazine grybeline infekcija.
Tuberkuliozė
Buvo pranešta apie tuberkuliozės atvejus pacientams, gydytiems Simponi. Reikėtų pažymėti, kad daugeliu atvejų tai buvo ekstrapulmoninė tuberkuliozė, tiek lokalizuota, tiek difuzinė.
Prieš pradedant gydymą Simponi, visi pacientai turi būti įvertinti, ar nėra aktyvios ir neaktyvios („latentinės“) tuberkuliozės. Į šį vertinimą turėtų būti įtraukta išsami ligos istorija, įskaitant asmeninę tuberkuliozės istoriją arba galimą ankstesnį kontaktą su tuberkuliozės infekcijos šaltiniu ir ankstesnį ir (arba) kartu vartojamą imunosupresinį gydymą. Visiems pacientams reikia atlikti atitinkamus diagnostinius tyrimus, tokius kaip odos ar kraujo tuberkulino tyrimai ir krūtinės ląstos rentgeno nuotraukos (gali būti taikomos vietinės gairės). Rekomenduojama apie šiuos tyrimus pranešti paciento įspėjimo kortelėje.Skiriantiems gydytojams primenama apie klaidingai neigiamų tuberkulino odos tyrimų rezultatų riziką, ypač sunkiai sergantiems ar susilpnėjusio imuniteto pacientams.
Jei diagnozuota aktyvi tuberkuliozė, gydymo Simponi negalima pradėti (žr. 4.3 skyrių).
Jei įtariama latentinė tuberkuliozė, reikia pasikonsultuoti su gydytoju, turinčiu tuberkuliozės gydymo patirties. Visais toliau aprašytais atvejais reikia atidžiai apsvarstyti gydymo Simponi naudos ir rizikos santykį.
Jei diagnozuojama neaktyvi („latentinė“) tuberkuliozė, prieš pradedant gydymą Simponi, prieš pradedant gydymą Simponi, reikia pradėti gydymą nuo latentinės tuberkuliozės.
Pacientams, kuriems yra daug ar reikšmingų tuberkuliozės rizikos veiksnių ir kurių latentinės tuberkuliozės testas yra neigiamas, prieš pradedant Simponi, reikia apsvarstyti gydymą nuo tuberkuliozės. Prieš pradedant gydymą Simponi, taip pat reikia apsvarstyti galimybę naudoti gydymą nuo tuberkuliozės pacientai, anksčiau sirgę latentine ar aktyvia tuberkulioze, kuriems negalima patvirtinti tinkamo gydymo kurso.
Aktyvios tuberkuliozės atvejų pasitaikė pacientams, gydytiems Simponi latentinės tuberkuliozės gydymo metu ir po jo. Simponi gydomus pacientus reikia atidžiai stebėti dėl aktyvios tuberkuliozės požymių ir simptomų, įskaitant pacientus, kurių latentinės tuberkuliozės testas buvo neigiamas, pacientus, kurie gydomi nuo latentinės tuberkuliozės, arba pacientus, kurie anksčiau buvo gydomi nuo latentinės tuberkuliozės. "Tuberkuliozės infekcija.
Visiems pacientams reikia patarti kreiptis į gydytoją, jei gydymo Simponi metu arba po jo atsiranda tuberkuliozės požymių / simptomų (pvz., Nuolatinis kosulys, išsekimas / svorio kritimas, silpna temperatūra).
Hepatito B viruso reaktyvavimas
Buvo pastebėta hepatito B reaktyvacija pacientams, gydytiems TNF antagonistais, įskaitant Simponi, ir kurie buvo lėtiniai šio viruso nešiotojai (ty teigiami paviršiaus antigenai). Kai kuriais atvejais buvo mirtinų pasekmių.
Prieš pradedant gydymą Simponi, pacientus reikia ištirti dėl HBV infekcijos. Pacientams, kurių HBV infekcija yra teigiama, rekomenduojama pasitarti su gydytoju, turinčiu patirties gydant hepatitą B.
Hepatito B viruso nešiotojus, kuriems reikia gydyti Simponi, reikia atidžiai stebėti dėl aktyvios hepatito B viruso infekcijos požymių ir simptomų gydymo metu ir daugelį mėnesių po gydymo pabaigos. Turima pakankamai duomenų apie pacientus, sergančius hepatito B virusu, gydomus antivirusiniais vaistais. kartu su TNF antagonistais, siekiant užkirsti kelią hepatito B viruso reaktyvacijai. Pacientams, kuriems pasireiškia hepatito B viruso reaktyvacija, gydymą Simponi reikia nutraukti ir pradėti veiksmingą antivirusinį gydymą ir pradėti tinkamą palaikomąjį gydymą.
Piktybiniai navikai ir limfoproliferacinės ligos
Galimas TNF inhibitorių terapijos vaidmuo kuriant piktybinius navikus nežinomas. Remiantis turimomis žiniomis, negalima atmesti galimos limfomos, leukemijos ar kitų piktybinių navikų išsivystymo rizikos pacientams, gydomiems TNF antagonistu. Svarstant gydymą TNF inhibitoriais, pacientams, kuriems yra buvęs piktybinis navikas, arba atsargiai tęsti gydymą pacientams, kuriems pasireiškia piktybinis navikas, reikia būti atsargiems.
Piktybiniai vaikų navikai
Po vaistinio preparato patekimo į rinką buvo pranešta apie piktybinius navikus, kai kuriais atvejais mirtinus, tarp vaikų, paauglių ir jaunų suaugusiųjų (iki 22 metų), gydytų TNF blokatoriais (gydymo pradžia ≤ 18 metų) Maždaug pusė atvejų buvo Kiti atvejai buvo įvairių piktybinių navikų, įskaitant retus piktybinius navikus, dažniausiai susijusius su imunosupresija. Negalima atmesti piktybinių navikų išsivystymo rizikos vaikams ir paaugliams, gydomiems TNF inhibitoriais.
Limfoma ir leukemija
Kontroliuojamose klinikinių tyrimų su visais TNF inhibitoriais, įskaitant Simponi, etapuose, daugiau limfomos atvejų buvo pastebėta tarp pacientų, kurie buvo gydomi anti-TNF, palyginti su kontroliniais pacientais. IIb ir III fazės klinikinių Simoni gydymo RA, AP ir SA metu tyrimų metu Simponi gydytiems pacientams limfomos dažnis buvo didesnis nei tikėtasi bendroje populiacijoje. Simponi gydytiems pacientams buvo pranešta apie leukemijos atvejus. padidėjusi limfomos ir leukemijos rizika pacientams, sergantiems reumatoidiniu artritu, kuriems yra ilga, labai aktyvi uždegiminė liga, o tai apsunkina rizikos įvertinimą.
Po pateikimo į rinką buvo pranešta apie retus hepatospleninės T-ląstelių limfomos (HSTCL) atvejus pacientams, gydytiems kitais TNF blokatoriais (žr. 4.8 skyrių). Ši reta T-ląstelių limfomos forma yra labai agresyvi ir dažniausiai baigiasi mirtimi Dauguma atvejų pasireiškė paaugliams ir jauniems suaugusiems vyrams, beveik visiems kartu gydant azatioprinu (AZA) arba 6-merkaptopurinu (6-MP) nuo žarnyno uždegimo. Reikia atidžiai apsvarstyti galimą AZA arba 6-MP ir Simponi derinio riziką.Negalima atmesti hepatospleninės T-ląstelių limfomos išsivystymo rizikos pacientams, gydomiems TNF blokatoriais.
Piktybiniai navikai, išskyrus limfomą
Kontroliuojamuose IIb ir III fazės klinikinių tyrimų su Simponi RA, AP, SA ir CU etapuose kitų piktybinių navikų, išskyrus limfomą (išskyrus nemelanominį odos vėžį), dažnis buvo panašus tarp Simponi ir kontrolinės grupės .
Storosios žarnos displazija / karcinoma
Nežinoma, ar gydymas golimumabu turi įtakos displazijos ar gaubtinės žarnos vėžio atsiradimo rizikai. Visi pacientai, sergantys opiniu kolitu, kuriems yra didesnė rizika susirgti gaubtinės žarnos displazija ar karcinoma (pvz., Pacientai, sergantys ilgalaikiu opiniu kolitu ar pirminiu sklerozuojančiu cholangitu) arba kurie anksčiau sirgo displazija ar gaubtinės žarnos vėžiu, turi būti ištirti dėl šios displazijos. reguliariais intervalais prieš pradedant gydymą ir ligos eigoje. Į šį įvertinimą turėtų būti įtraukta kolonoskopija ir biopsijos pagal vietines rekomendacijas. Pacientams, kuriems neseniai diagnozuota displazija, gydomi Simponi, reikia atidžiai apsvarstyti pavojaus ir naudos santykį kiekvienam pacientui ir ar tęsti gydymą.
Atliekant tiriamąjį klinikinį tyrimą, kuriame buvo vertinamas Simponi vartojimas pacientams, sergantiems sunkia nuolatine astma, Simponi gydytiems pacientams buvo pranešta apie daugiau piktybinių navikų atvejų nei kontroliniams pacientams (žr. 4.8 skyrių). Šių išvadų reikšmė nežinoma.
Atliekant tiriamąjį klinikinį tyrimą, kuriame buvo vertinamas kito anti-TNF agento, infliksimabo, vartojimas pacientams, sergantiems vidutinio sunkumo ar sunkia lėtine obstrukcine plaučių liga (LOPL), buvo pranešta apie daugiau piktybinių navikų atvejų. Visi pacientai ilgą laiką rūkė, todėl reikia atsargiai vertinti TNF antagonisto vartojimą LOPL sergantiems pacientams, taip pat pacientams, kuriems yra padidėjusi piktybinių navikų rizika.
Odos navikai
Buvo pranešta apie melanomą ir Merkel ląstelių karcinomą pacientams, gydytiems TNF slopinančiais preparatais, įskaitant Simponi (žr. 4.8 skyrių). Rekomenduojama periodiškai tikrinti odą, ypač pacientams, turintiems odos vėžio rizikos veiksnių.
Stazinis širdies nepakankamumas (CHF)
Gauta pranešimų apie stazinio širdies nepakankamumo (ŠKL) pablogėjimą ir naujų širdies nepakankamumo atvejų vartojant TNF antagonistus, įskaitant Simponi. Kai kurie atvejai baigėsi mirtinai. Klinikinio tyrimo su kitu TNF antagonistu metu buvo pastebėtas stazinio širdies nepakankamumo pablogėjimas ir padidėjęs mirtingumas dėl širdies nepakankamumo. Simponi netirtas pacientams, sergantiems širdies nepakankamumu. Simponi reikia atsargiai skirti pacientams, kuriems yra nepakankamumas. Širdies nepakankamumas (lengva NYHA klasė) / II) Pacientus, kuriems pasireiškia nauji ar blogėja širdies nepakankamumo simptomai, reikia atidžiai stebėti ir Simponi gydymą nutraukti (žr. 4.3 skyrių).
Poveikis nervų sistemai
TNF blokuojančių vaistinių preparatų, įskaitant Simponi, vartojimas buvo susijęs su naujais klinikinių simptomų ir (arba) centrinės nervų sistemos demielinizuojančių sutrikimų, įskaitant išsėtinės sklerozės ir periferinių demielinizavimo sutrikimų, radiografinių požymių atsiradimu ar paūmėjimu. prieš pradedant gydymą Simponi, reikia atidžiai apsvarstyti gydymo nuo TNF naudą ir riziką.
Atsiradus šiai būklei, reikia apsvarstyti galimybę nutraukti gydymą Simponi (žr. 4.8 skyrių).
Chirurginės intervencijos
Gydymo Simponi saugumo pacientams, kuriems buvo atlikta operacija, įskaitant artroplastiką, patirties yra nedaug.Planuojant operaciją reikia atsižvelgti į ilgą pusinės eliminacijos laiką. Pacientą, kuriam gydymo Simponi metu reikia operacijos, reikia atidžiai stebėti, ar nėra padidėjusi infekcijų rizika, ir apsvarstyti tinkamas priemones.
Imunosupresija
Yra galimybė, kad vaistai nuo TNF, įskaitant Simponi, veikia šeimininko apsaugą nuo infekcijų ir piktybinių navikų, nes TNF tarpininkauja uždegimui ir moduliuoja ląstelių imuninį atsaką.
Autoimuninės reakcijos
Santykinis TNF trūkumas? dėl gydymo nuo TNF, gali prasidėti autoimuninis procesas. Jei po gydymo Simponi pacientui pasireiškia simptomai, prognozuojantys vilkligės tipo sindromą, ir teigiamas dvigubų DNR antikūnų buvimas, gydymą Simponi reikia nutraukti ( žr. 4.8 skyrių).
Hematologinės reakcijos
Po vaistinio preparato patekimo į rinką gauta pranešimų apie pancitopenijos, leukopenijos, neutropenijos, aplastinės anemijos ir trombocitopenijos atvejus pacientams, gydytiems anti-TNF vaistais. Klinikinių Simponi tyrimų metu nebuvo dažnai pranešta apie citopenijas, įskaitant pancitopeniją. Visiems pacientams reikia patarti nedelsiant kreiptis į gydytoją, jei jiems atsiranda suderinami kraujo diskrazijos požymiai ar simptomai (pvz., Nuolatinis karščiavimas, kraujosruvos, kraujavimas ir blyškumas). Pacientams, kuriems patvirtinti reikšmingi hematologiniai sutrikimai, reikia apsvarstyti galimybę nutraukti gydymą Simponi.
Kartu vartojami TNF antagonistai ir anakinra
Kombinuotuose klinikiniuose anakinros ir kito TNF inhibitoriaus etanercepto tyrimuose, be papildomos klinikinės naudos, pasireiškė sunkios infekcijos ir neutropenija. Atsižvelgiant į nepageidaujamų reiškinių, pastebėtų taikant šį kombinuotą gydymą, panašų toksiškumą gali atsirasti vartojant anakinros ir kitų TNF inhibitorių. Simponi ir anakinros derinys nerekomenduojamas.
Kartu skiriant TNF antagonistus ir abataceptą
Klinikinių tyrimų metu kartu vartojant TNF antagonistus ir abataceptą, padidėjo infekcijų, įskaitant sunkias infekcijas, rizika, palyginti su vartojamais vien TNF antagonistais, tačiau klinikinė nauda nepadidėjo. Simponi ir abatacepto nerekomenduojama.
Vartojimas kartu su kitomis biologinėmis terapijomis
Nėra pakankamai informacijos apie Simponi vartojimą kartu su kitomis biologinėmis terapijomis, kuriomis gydomos tos pačios ligos, kaip ir Simponi. Simponi vartoti kartu su šiais biologiniais preparatais nerekomenduojama dėl padidėjusios infekcijos rizikos ir kitų galimų vaistų sąveikų.
Biologinių DMARD pakeitimas
Reikėtų būti atsargiems ir toliau stebėti pacientus, kai jie keičiasi iš vieno biologinio į kitą, nes sutampanti biologinė veikla gali dar labiau padidinti nepageidaujamų reiškinių, įskaitant infekciją, riziką.
Skiepai / infekcinės terapinės medžiagos
Simponi gydomi pacientai gali būti skiepijami kartu, išskyrus gyvas vakcinas (žr. 4.5 ir 4.6 skyrius). Pacientų, gydomų anti-TNF terapija, duomenų apie atsaką į skiepijimą, gyvas vakcinas arba antrinį infekcijos perdavimą skiriant gyvas vakcinas yra nedaug. Naudojant gyvas vakcinas gali atsirasti klinikinių infekcijų, įskaitant infekcijų plitimą .
Kiti infekcinių terapinių agentų, tokių kaip gyvos susilpnintos bakterijos, naudojimas (pvz., Į veną įlašinamas BCG vėžio gydymui) gali sukelti klinikines infekcijas, įskaitant išplitusias infekcijas. Rekomenduojama kartu su Simponi neskirti gydomųjų infekcinių agentų.
Alerginės reakcijos
Patekus į rinką, buvo pranešta apie sunkias sistemines padidėjusio jautrumo reakcijas (įskaitant anafilaksinę reakciją), pavartojus Simponi. Kai kurios iš šių reakcijų pasireiškė pirmą kartą pavartojus Simponi. Jei pasireiškia anafilaksinė ar kita alerginė reakcija, Simponi vartojimą reikia nedelsiant nutraukti ir pradėta tinkama terapija.
Jautrumas lateksui
Užpildyto švirkštiklio arba užpildyto švirkšto adatos dangtelis pagamintas iš latekso, kuriame yra džiovintos natūralios gumos, ir gali sukelti alergines reakcijas lateksui jautriems asmenims.
Specialios populiacijos
Senyvi žmonės (≥ 65 metų)
III fazės RA, AP, SA ir CU tyrimuose 65 metų ir vyresniems pacientams, gydytiems Simponi, bendrų nepageidaujamų reiškinių (AE), sunkių nepageidaujamų reiškinių (EAG) ir sunkių infekcijų skirtumų nepastebėta. jaunesniems pacientams. Tačiau reikia būti atsargiems gydant vyresnio amžiaus žmones ir ypatingą dėmesį skirti infekcijų atsiradimui .. Ašiniame SpA tyrime Nr.
Inkstų ir kepenų funkcijos sutrikimas
Specifinių Simponi tyrimų su pacientais, kurių inkstų ar kepenų funkcija sutrikusi, neatlikta. Simponi reikia atsargiai vartoti asmenims, kurių kepenų funkcija sutrikusi (žr. 4.2 skyrių).
Vaikų populiacija
Vakcinos
Jei įmanoma, rekomenduojama, kad prieš pradedant gydymą Simponi, pediatriniai pacientai būtų nuolat atnaujinami ir skiepijami pagal galiojančias skiepijimo gaires.
Pagalbinės medžiagos
Simponi sudėtyje yra sorbitolio (E420). Pacientai, kuriems nustatytas retas paveldimas fruktozės netoleravimas, neturėtų vartoti Simponi.
Galimos gydymo klaidos
Simponi yra registruotas 50 mg ir 100 mg stiprumu po oda. Svarbu, kad būtų vartojama teisinga dozė, kaip nurodyta dozavimo metu (žr. 4.2 skyrių). Reikia pasirūpinti tinkama doze, kad pacientai nebūtų perdozuoti ar perdozuoti.
04.5 Sąveika su kitais vaistiniais preparatais ir kitos sąveikos formos
Sąveikos tyrimų neatlikta.
Vartojimas kartu su kitomis biologinėmis terapijomis
Simponi nerekomenduojama derinti su kitomis biologinėmis terapijomis, kuriomis gydomos tos pačios ligos, kaip ir Simponi, įskaitant anakinrą ir abataceptą (žr. 4.4 skyrių).
Gyvos vakcinos / infekcinės terapinės medžiagos
Gyvų vakcinų negalima skirti kartu su Simponi (žr. 4.4 ir 4.6 skyrius).
Infekcinių terapinių preparatų negalima skirti kartu su Simponi (žr. 4.4 skyrių).
Metotreksatas
Nors kartu vartojant metotreksatą (MTX) pacientams, sergantiems RA, AP ar AS, padidėja vienodos koncentracijos pusiausvyros būsenos koncentracija, duomenys nerodo, kad reikia keisti Simponi dozę arba MTX (žr. 5.2 skyrių).
04.6 Nėštumas ir žindymo laikotarpis
Vaisingo amžiaus moterys
Vaisingos moterys turi naudoti tinkamas kontracepcijos priemones, kad išvengtų nėštumo, ir tęsti vartojimą mažiausiai 6 mėnesius po paskutinio golimumabo vartojimo.
Nėštumas
Nėra pakankamai duomenų apie golimumabo vartojimą nėščioms moterims. Kadangi golimumabas slopina TNF, jo vartojimas nėštumo metu gali paveikti normalų naujagimio imuninį atsaką. Tyrimai su gyvūnais nerodo tiesioginio ar žalingo poveikio. Netiesioginis poveikis nėštumui , embriono / vaisiaus vystymasis, gimdymas ar pogimdyminis vystymasis (žr. 5.3 skyrių) .Golimumabo nerekomenduojama vartoti nėščioms moterims; golimumabą nėščioms moterims galima skirti tik tada, kai to tikrai reikia.
Golimumabas kerta placentą. Po gydymo TNF slopinančiu monokloniniu antikūnu nėštumo metu antikūnas buvo rastas iki 6 mėnesių kūdikių, gimusių gydomoms moterims, serume, todėl šiems kūdikiams gali padidėti infekcijos rizika.
Gyvų vakcinų skiepijimas paveiktiems kūdikiams gimdoje golimumabo nerekomenduojama vartoti 6 mėnesius po paskutinės motinos golimumabo injekcijos nėštumo metu (žr. 4.4 ir 4.5 skyrius).
Žindymas
Nežinoma, ar golimumabas patenka į motinos pieną, ar absorbuojamas sistemiškai. Nurodyta, kad golimumabas patenka į beždžionių pieną ir kadangi žmogaus imunoglobulinai išsiskiria į pieną, gydymo metu ir mažiausiai 6 mėnesius moterys neturėtų žindyti. po gydymo golimumabu.
Vaisingumas
Golimumabo vaisingumo tyrimų su gyvūnais neatlikta. Vaisingumo tyrimas su pelėmis, naudojant panašų antikūną, selektyviai slopinantį pelių TNF funkcinį aktyvumą, neparodė jokio reikšmingo poveikio vaisingumui (žr. 5.3 skyrių).
04.7 Poveikis gebėjimui vairuoti ir valdyti mechanizmus
Simponi gali šiek tiek sutrikdyti gebėjimą vairuoti ir valdyti mechanizmus.Pavartojus Simponi gali svaigti galva (žr. 4.8 skyrių).
04.8 Nepageidaujamas poveikis
Saugos profilio santrauka
Pagrindinių RA, AP, SA, Axial SpA nr ir CU tyrimų kontroliniu laikotarpiu viršutinė kvėpavimo takų infekcija buvo dažniausia nepageidaujama reakcija į vaistą (ADR), apie kurią pranešta 12,6% golimumabu gydytų pacientų, palyginti su 11,0% kontroliuoti pacientus. Sunkiausi golimumabo nepageidaujami reiškiniai yra sunkios infekcijos (įskaitant sepsį, pneumoniją, tuberkuliozę, invazines grybelines infekcijas ir oportunistines infekcijas), demielinizuojančios ligos, HBV reaktyvacija, ŠKL, autoimuniniai procesai (į vilkligę panašus sindromas), hematologinės reakcijos, sunkus padidėjusio jautrumo sisteminis ( (įskaitant anafilaksinę reakciją), vaskulitą, limfomą ir leukemiją (žr. 4.4 skyrių).
Lentelė su nepageidaujamų reakcijų sąrašu
Nepageidaujamos reakcijos, pastebėtos klinikinių tyrimų metu ir apie kurias pranešta po golimumabo vartojimo visame pasaulyje, išvardytos 1 lentelėje. Organų sistemų klasėje nepageidaujamos reakcijos į vaistą išvardytos pagal dažnumą, naudojant šias kategorijas: labai dažni (≥ 1/10); dažni (≥ 1/100,
1 lentelė
Lentelė su NRV sąrašu
*: Stebima kartu su kitomis TNF blokuojančiomis medžiagomis.
Šiame skyriuje visų golimumabo vartojimo stebėjimų trukmės mediana (maždaug 4 metai) paprastai pateikiama. Kai golimumabo vartojimą apibūdina dozė, vidutinė stebėjimo trukmė skiriasi (maždaug 2 metai, kai vartojama 50 mg dozė, ir maždaug 3 metai, kai vartojama 100 mg dozė), nes pacientus galima keisti viena doze.
Pasirinktų nepageidaujamų reakcijų į vaistą aprašymas
Infekcijos
Pagrindinių tyrimų kontroliniu laikotarpiu viršutinių kvėpavimo takų infekcija buvo dažniausia nepageidaujama reakcija, apie kurią pranešta 12,6% golimumabu gydytų pacientų (dažnis 100 tiriamųjų metų: 60,8; 95% PI: 55,0, 67,1), palyginti su 11,0% kontrolinių pacientų (dažnis 100 tiriamųjų per metus: 54,5; 95% PI: 46,1, 64,0). Kontroliuojamose ir nekontroliuojamose tyrimo fazėse, kurių vidutinis stebėjimas buvo maždaug 4 metai, viršutinių kvėpavimo takų infekcijų dažnis 100 tiriamųjų metų buvo 34,9 atvejo; 95% PI: 33,8, 36,0 golimumabu gydytų pacientų.
Pagrindinių tyrimų kontroliniu laikotarpiu infekcijos buvo pastebėtos 23,0% golimumabu gydytų pacientų (dažnis 100 tiriamųjų metų: 132,0; 95% PI: 123,3, 141,1), palyginti su 20,2% kontrolinių pacientų (dažnis 100 tiriamųjų metų: 122,3; 95% PI: 109,5, 136,2). Kontroliuojamose ir nekontroliuojamose tyrimo fazėse, kurių vidutinis stebėjimas buvo maždaug 4 metai, infekcijų dažnis 100 tiriamųjų metų buvo 81,1 atvejo; 95% PI: 79,5, 82,8 golimumabu gydytų pacientų.
RA, AP, SA ir Axial SpA nr tyrimų kontroliniu laikotarpiu sunkios infekcijos buvo pastebėtos 1,2% golimumabu gydytų pacientų ir 1,2% kontrolinių pacientų. Sunkių infekcijų dažnis per 100 tiriamųjų metų stebint RA, AP, SA ir nr-Axial SpA tyrimų laikotarpį buvo 7,3; 95% PI: 4,6, 11, 1 100 mg golimumabo grupėje , 2,9; 95% PI: 1,2, 6,0 golimumabo 50 mg grupei ir 3,6; 95% PI: 1, 5, 7,0 placebo grupei. 0,8% golimumabu gydytų pacientų, palyginti su 1,5% kontrolinių pacientų. Sunkios infekcijos, pastebėtos golimumabu gydytiems pacientams, buvo tuberkuliozė, bakterinės infekcijos, įskaitant sepsį ir pneumoniją, invazinės grybelinės infekcijos ir kitos oportunistinės infekcijos. Kai kurios iš šių infekcijų buvo mirtinos. Kontroliuojamose ir nekontroliuojamose pagrindinių tyrimų, kurių vidutinis stebėjimas buvo iki 3 metų, dalyse sunkių infekcijų, įskaitant oportunistines infekcijas ir tuberkuliozę, dažnis buvo didesnis pacientams, gydytiems 100 mg golimumabu, nei gydytiems golimumabu. 50 mg 100 sunkių infekcijų atvejų 100 tiriamųjų metų buvo 4,1; 95% PI: 3,6, 4,5, pacientams, gydytiems 100 mg ir 2,5 golimumabu; 95% PI: 2,0, 3,1, pacientams, gydytiems 50 mg golimumabu.
Piktybiniai navikai
Limfoma
Svarbiausių tyrimų metu golimumabu gydytiems pacientams limfomos dažnis buvo didesnis nei tikėtasi. Kontroliuojamose ir nekontroliuojamose šių tyrimų dalyse, kurių vidutinis stebėjimas buvo iki 3 metų, buvo pastebėtas didesnis limfomos dažnis pacientams, gydytiems 100 mg golimumabu, palyginti su pacientais, gydytais 50 mg golimumabu. Limfoma buvo diagnozuota 11 tiriamųjų (1 iš 50 mg golimumabo ir 10 golimumabo 100 mg gydymo grupių), kurių dažnis (95% PI) 100 tiriamųjų metų stebint 0,03 ir 0,13 įvykio, atitinkamai vartojant 50 mg golimumabo ir 100 mg golimumabo, ir 0,00 įvykių placebą. Dauguma limfomų pasireiškė GO-AFTER tyrime, į kurį buvo įtraukti pacientai, anksčiau vartoję anti-TNF vaistus, kurių ligos trukmė buvo ilgesnė ir sunkesnė (žr. 4.4 skyrių).
Piktybiniai navikai, išskyrus limfomą
Pagrindinių tyrimų kontroliniais laikotarpiais ir maždaug 4 metų stebėjimo laikotarpiu kitų piktybinių navikų, išskyrus limfomą (išskyrus nemelanomos odos vėžį), dažnis tarp golimumabo ir kontrolinių grupių buvo panašus. Maždaug 4 metų stebėjimo laikotarpis, ne limfomos piktybinių navikų (išskyrus nemelanominį odos vėžį) dažnis buvo panašus į bendrą populiaciją.
Kontroliuojamame ir nekontroliuojamame pagrindinių tyrimų, kurių vidutinis stebėjimas buvo iki 3 metų, laikotarpiais ne melanomos odos vėžys buvo diagnozuotas 5 tiriamiesiems, gydytiems placebu, 10-50 mg golimumabo ir 31-100 mg golimumabo. dažnis (95% PI) per 100 stebėjimo metų-0,36 kombinuoto golimumabo ir 0,87-placebo.
Kontroliuojamame ir nekontroliuojamame pagrindinių tyrimų, kurių vidutinis stebėjimas buvo iki 3 metų, laikotarpiais, be melanomos, nemelanominio odos vėžio ir limfomos, piktybiniai navikai buvo diagnozuoti 5 tiriamiesiems, gydytiems placebu, 21 pacientui, gydytam golimumabu 50. mg ir 34 iš jų, gydytų 100 mg golimumabu, kurių dažnis (95% PI) per 100 stebėjimo metų buvo 0,48 kombinuoto golimumabo ir 0,87 placebo grupėje (žr. 4.4 skyrių).
Atvejai, apie kuriuos pranešta klinikinių tyrimų metu sergant astma
Atliekant tiriamąjį klinikinį tyrimą, pacientai, sergantys sunkia nuolatine astma, 0 savaitę gavo po oda šarminę golimumabo dozę (150% paskirtos gydymo dozės), po to 200 mg golimumabo, 100 mg golimumabo arba 50 mg golimumabo. 4 savaites po oda. buvo pranešta apie aštuonis piktybinius navikus golimumabo derinio grupėje (n = 230) ir nė vieną placebą (n = 79). 1 pacientui pasireiškė limfoma, 2 pacientams-nemelanominis odos vėžys, 5 pacientams-kiti piktybiniai navikai. Nebuvo jokio specifinio bet kokio tipo piktybinių navikų sujungimo.
Placebu kontroliuojamo tyrimo fazės metu visų piktybinių navikų dažnis (95% PI) per 100 stebėjimo metų buvo 3,19 golimumabo gydymo grupėje. Dažnis (95% PI) 100 stebėjimo metų -golimumabu gydomiems pacientams padidėjo 0,40 limfomos, 0,79-nemelanomos odos vėžio ir 1,99-kitų piktybinių navikų atveju. Tiriamiesiems, gydytiems placebu, šių piktybinių navikų dažnis (95% PI) 100 tiriamųjų per stebėjimo metus buvo 0,00. Šių išvadų reikšmė nežinoma.
Neurologiniai įvykiai
Kontroliuojamų ir nekontroliuojamų pagrindinių tyrimų metu, kai stebėjimo trukmė buvo vidutiniškai iki 3 metų, buvo pastebėta didesnė demielinizacijos rizika pacientams, gydytiems 100 mg golimumabu, palyginti su pacientais, gydytais 50 mg golimumabu (žr. 4.4 skyrių). .
Padidėjęs kepenų fermentų kiekis
Pagrindinių RA ir AP tyrimų kontroliniais laikotarpiais nedidelis ALT padidėjimas (> 1 ir 1 ir
Pagrindinių RA ir AS tyrimų kontroliniu laikotarpiu ALT padidėjimas ≥ 5 kartus viršija viršutinę normos ribą buvo retas ir buvo pastebėtas didesniam golimumabu gydytų pacientų skaičiui (0,4%iki 0, 9%), palyginti su kontroliniais pacientais (0,0%). Šios tendencijos nepastebėta AP populiacijoje. Kontroliuojamų ir nekontroliuojamų pagrindinių RA, AP ir SA tyrimų laikotarpiais, kurių vidutinis stebėjimas buvo 5 metai, ALT koncentracijos padidėjimas ≥ 5 kartus virš ULN buvo panašus tiek golimumabu gydytiems, tiek kontroliniams pacientams. Apskritai šie padidėjimai buvo besimptomiai, o anomalijos sumažėjo arba išnyko tęsiant ar nutraukiant golimumabo vartojimą arba keičiant kartu vartojamus vaistus. Kontroliuojamu ir nekontroliuojamu Axial SpA tyrimo laikotarpiu nebuvo pranešta apie atvejus. (Iki 1 metų) Pagrindinių CU indukcijos tyrimų su golimumabu laikotarpiais ALT padidėjimas ≥ 5 x VNR buvo stebimas panašiai tiek golimumabu, tiek placebu gydytiems pacientams (0, 3%-1,0%). Kontroliuojamu ir nekontroliuojamu pagrindinio UC laikotarpiu tyrimų, kurių vidutinis stebėjimas buvo maždaug 2 metai, pacientų, kurių ALT padidėjo ≥ 5 x VNR, dalis buvo 0,8 % pacientų, vartojusių golimumabą palaikomojo UC tyrimo laikotarpiu.
Atliekant pagrindinius RA, AP, SA ir ašinius SpA tyrimus, RA tyrimo pacientui, kuriam jau buvo kepenų sutrikimų ir golimumabu gydomų sutrikimų sukeliančių vaistų, atsirado mirtinas neinfekcinis hepatitas su gelta. Negalima atmesti golimumabo kaip prisidedančio ar sunkinančio veiksnio vaidmens.
Reakcijos injekcijos vietoje
Pagrindinių tyrimų kontroliniais laikotarpiais reakcijos injekcijos vietoje buvo pastebėtos 5,4% golimumabu gydytų pacientų, palyginti su 2,0% kontrolinės grupės pacientų. Antikūnų prieš golimumabą padidėjimas gali sukelti reakcijų injekcijos vietoje. Dauguma reakcijų injekcijos vietoje buvo lengvos ir vidutinio sunkumo, o dažniausiai pasireiškė eritema injekcijos vietoje. Paprastai reakcijos injekcijos vietoje nereikalauja nutraukti gydymo šiuo vaistu.
Kontroliuojamuose IIb ir / arba III fazės RA, AP, SA, ašinio SpA nr, sunkios nuolatinės astmos tyrimuose ir II / III fazės UC tyrimuose anafilaksinės reakcijos nepasireiškė nė vienam golimumabu gydytam pacientui.
Autoimuniniai antikūnai
Kontroliuojamame ir nekontroliuojamame pagrindinių tyrimų metu, kai buvo stebimi 1 metai, 3,5% golimumabu gydytų pacientų ir 2,3% kontrolinių pacientų neseniai buvo teigiamas ANA (titravimas 1: 160 arba didesnis). Anti-dsDNR antikūnų dažnis stebint vienerius metus anti-dsDNA neigiamiems pacientams iš pradžių buvo 1,1%.
Vaikų populiacija
Jaunatvinis idiopatinis poliartritinis artritas
Golimumabo saugumas buvo tiriamas III fazės tyrime, kuriame dalyvavo 173 pacientai, sergantys pJIA nuo 2 iki 17 metų. Vidutinis stebėjimas buvo maždaug dveji metai. Šiame tyrime nepageidaujamų reiškinių, apie kuriuos pranešta, tipas ir dažnis paprastai buvo panašūs į tuos, kurie buvo pastebėti atliekant tyrimus su RA sergančiais suaugusiais.
Pranešimas apie įtariamas nepageidaujamas reakcijas
Svarbu pranešti apie įtariamas nepageidaujamas reakcijas, atsiradusias po vaisto registravimo, nes tai leidžia nuolat stebėti vaisto naudos ir rizikos santykį. Sveikatos priežiūros specialistų prašoma pranešti apie bet kokias įtariamas nepageidaujamas reakcijas per Italijos vaistų agentūrą, svetainę: http://www.agenziafarmaco.gov.it/it/responsabili.
04.9 Perdozavimas
Klinikinio tyrimo metu į veną buvo suleistos vienkartinės dozės iki 10 mg / kg be jokio dozę ribojančio toksiškumo. Perdozavus, rekomenduojama stebėti, ar pacientui neatsiranda nepageidaujamų reiškinių požymių ir simptomų, ir nedelsiant pradėti tinkamą simptominį gydymą.
05.0 FARMAKOLOGINĖS SAVYBĖS
05.1 Farmakodinaminės savybės
Farmakoterapinė grupė: imunosupresantai, naviko nekrozės faktoriaus alfa (TNF-a) inhibitoriai, ATC kodas-L04AB06
Veiksmo mechanizmas
Golimumabas yra žmogaus monokloninis antikūnas, kuris sudaro stabilius kompleksus, turinčius didelį afinitetą tirpioms ir bioaktyvioms TNF-α transmembraninėms formoms. žmogaus, užkertant kelią TNF- surišimui. prie jo receptorių.
Farmakodinaminis poveikis
Įrodyta, kad golimumabo prisijungimas prie žmogaus TNF slopina TNF-a sukeltą adhezijos molekulių, selektino E, 1 tipo kraujagyslių ląstelių sukibimo molekulės (VCAM) ir 1 tipo intracelulinės adhezijos molekulės (ICAM) ekspresiją ląstelių paviršiuje žmogaus endotelio ląstelėse. In vitroTaip pat golimumabas slopino TNF sukeltą sekreciją, kurią sukelia interleukino (IL) -6, IL-8 ir granulocitų bei makrofagų kolonijas stimuliuojantis faktorius (GM-CSF) žmogaus endotelio ląstelėse.
Buvo pastebėtas C reaktyvaus baltymo (CRP) lygio pagerėjimas, palyginti su placebo grupėmis, o gydymas Simponi žymiai sumažino serumo koncentraciją, palyginti su pradiniu IL-6, ICAM-1, matricos metaloproteinazės.3 (MMP) ir kraujagyslių endotelio kiekiu. augimo faktorius (VEGF), palyginti su kontroliniu gydymu. Be to, RA ir AS pacientams TNF-? sumažėjo ir IL-8 lygis sumažėjo pacientams, sergantiems AP. Šie pokyčiai buvo pastebėti per pirmąjį vertinimą (4 savaitę) po pirminio Simponi vartojimo ir paprastai truko iki 24 savaitės.
Klinikinis veiksmingumas
Reumatoidinis artritas
Simponi veiksmingumas buvo įrodytas trijuose daugiacentriuose, atsitiktinių imčių, dvigubai akluose, placebu kontroliuojamuose klinikiniuose tyrimuose, kuriuose dalyvavo daugiau kaip 1500 ≥ 18 metų pacientų, sergančių vidutinio sunkumo ar sunkiu aktyviu RA, remiantis Amerikos reumatologijos kolegijos (ACR) kriterijais. ) mažiausiai 3 mėnesius prieš atranką.Pacientams turėjo būti bent 4 patinę ir 4 skausmingi sąnariai. Simponi arba placebas buvo švirkščiamas po oda kas 4 savaites.
GO-FORWARD įvertino 444 pacientus, sergančius aktyviu RA, nepaisant stabilios mažiausiai 15 mg per savaitę MTX dozės ir kurie anksčiau nebuvo gydomi jokiais vaistais nuo TNF. Pacientai buvo atsitiktinai suskirstyti į placebą + MTX, Simponi 50 mg + MTX, Simponi 100 mg + MTX arba Simponi 100 mg + placebą. Pacientai, vartoję placebą + MTX, po 24 savaitės buvo paskirti 50 mg Simponi + MTX. 52 savaitę pacientai dalyvavo atvirame ilgalaikio pratęsimo tyrime.
GO-AFTER įvertino 445 pacientus, anksčiau gydytus vienu ar daugiau vaistų nuo TNF, adalimumabo, etanercepto ar infliksimabo. Pacientai buvo atsitiktinai suskirstyti į placebą, 50 mg Simponi arba 100 mg Simponi. Tyrimo metu pacientai galėjo tęsti gydymą DMARD kartu su MTX, sulfasalazinu (SSZ) ir (arba) hidroksichlorokvinu (HCQ). Ankstesnės anti-TNF terapijos nutraukimo priežastys buvo neveiksmingumas (58%), netoleravimas (13%) ir (arba) kitos priežastys nei saugumas ar veiksmingumas (29%, daugiausia dėl finansinių priežasčių).
GO-BEFORE įvertino 637 pacientus, sergančius aktyviu RA, MTX anksčiau negydytą ir anksčiau negydytą vaistu nuo TNF. Pacientai buvo atsitiktinai parinkti, kad gautų placebą + MTX, Simponi 50 mg + MTX, Simponi 100 mg + MTX arba Simponi 100 mg + placebą. 52 savaitę pacientai dalyvavo atvirame ilgalaikio pratęsimo tyrime, kuriame pacientai, vartoję placebą + MTX ir turėję bent 1 skausmingą ar patinusį sąnarį, buvo perkelti į gydymą Simponi 50 mg + MTX.
„GO-FORWARD“ pagrindiniai (bendri) baigtiniai rodikliai buvo pacientų, pasiekusių atsaką į ACR 20, procentas 14 savaitę ir sveikatos vertinimo klausimyno (HAQ) pagerėjimas 24 savaitę, palyginti su pradiniu. GO-AFTER pagrindinė baigtis buvo pacientų, kuriems ACR 20 atsakas buvo pasiektas 14 savaitę. GO-BEFORE pagrindiniai kriterijai buvo pacientų, kurie 24 savaitę pasiekė ACR 50 atsaką, dalis ir van der Heijde (vdH) modifikuoto Sharp balo pokytis nuo pradinio lygio (vdH). Be pirminių baigčių, buvo papildomai įvertintas Simponi gydymo poveikis artrito požymiams ir simptomams, rentgeno atsakui, fizinei funkcijai ir gyvenimo būklei.
Apskritai kliniškai reikšmingų veiksmingumo vertinimo skirtumų tarp Simponi 50 mg ir 100 mg derinio su MTX dozavimo režimais nepastebėta iki 104 savaitės GO-FORWARD ir GO-BEFORE ir iki 24 savaitės. iš RA tyrimų pagal tyrimo planą, pacientai, kuriems buvo pratęstas ilgalaikis gydymas, gydytojo nuožiūra gali būti pakeisti 50 mg Simponi ir 100 mg dozėmis.
ženklai ir simptomai
Pagrindiniai ACR kriterijų rezultatai vartojant Simponi 50 mg dozę 14, 24 ir 52 savaitėmis GO-FORWARD, GO-AFTER ir GO-BEFORE yra pateikti 2 lentelėje ir aprašyti žemiau. Atsakymai buvo pastebėti per pirmąjį vertinimą (4 savaitę) po pirminio Simponi vartojimo.
GO-FORWARD tyrime iš 89 tiriamųjų, atsitiktinai atrinktų Simponi 50 mg + MTX, 104-ąją savaitę dar buvo gydomi 48 iš jų. Tarp jų 40, 33 ir 24 pacientai 104 savaitę turėjo ACR 20/50/70 atsaką, Tarp pacientų, kurie liko tyrime ir gydomi Simponi, panašus ACR 20/50/70 atsako dažnis buvo stebimas nuo 104 iki 256 savaitės.
GO-AFTER tyrimo metu pacientų, kuriems buvo pasiektas atsakas į ACR 20, procentas buvo didesnis tarp Simponi gydytų pacientų, palyginti su placebą vartojusiais pacientais, neatsižvelgiant į nurodytą priežastį nutraukti vieną ar kelis priešuždegiminius gydymo būdus.
2 lentelė
Pagrindiniai veiksmingumo rezultatai, gauti iš kontroliuojamų GO-FORWARD, GO-AFTER ir GO-BEFORE dalių.
a n atitinka atsitiktinių imčių pacientus; faktinis pacientų skaičius, kurį galima įvertinti pagal kiekvieną galutinį rezultatą, gali skirtis priklausomai nuo laiko.
* p ≤ 0,001
NA: Netaikoma
GO-BEFORE tyrimo metu pirminė analizė pacientams, sergantiems vidutinio sunkumo ar sunkiu reumatoidiniu artritu (Simponi 50 ir 100 mg + MTX derinio grupės, palyginti su vien MTX, vartojant ACR 50), 24 savaitę nebuvo statistiškai reikšminga (p = 0,053 52 savaitę) populiacijos, Simponi 50 mg + MTX grupės pacientų, kuriems pasireiškė ACR atsakas, dalis paprastai buvo didesnė, bet labai nesiskyrė, palyginti su vien MTX (žr. 2 lentelę). Papildomos pogrupių analizės, reprezentuojančios nurodytą pacientų grupę , aktyvus ir progresuojantis RA. Paprastai geresnis poveikis buvo įrodytas vartojant Simponi 50 mg + MTX, palyginti su vien tik MTX nurodytoje populiacijoje, palyginti su visa populiacija.
GO-FORWARD ir GO-AFTER tyrimuose statistiškai ir kliniškai reikšmingas atsakas į ligos aktyvumo skalę (DAS28) buvo pastebėtas kiekviename iš anksto nustatytame etape, 14 ir 24 savaitę (p ≤ 0,001). Tarp pacientų, kurie ir toliau vartojo Simponi, atsitiktinių imčių tyrimo pradžioje, DAS28 atsakas išliko iki 104 savaitės. Tarp pacientų, kurie liko tyrime ir buvo gydomi Simponi, DAS28 atsakas buvo panašus nuo 104 iki 256 savaitės.
GO-BEFORE tyrimo metu buvo įvertintas pagrindinis klinikinis atsakas, kuris apibrėžiamas kaip ACR 70 atsako palaikymas nuolatinį 6 mėnesių laikotarpį. 52 savaitę 15% Simponi 50 mg + MTX grupės pacientų pasiekė geresnį klinikinį atsaką, palyginti su 7% pacientų, vartojusių placebą ir MTX (p = 0,018). Iš 159 tiriamųjų, atsitiktinai parinktų Simponi 50 mg + MTX, 104 savaitę dar buvo gydomi. Tarp šių 85, 66, 66 ir 53 pacientų AKR atsakas buvo atitinkamai 104 savaitę ir gydytas Simponi, panašiai ACR 20/50/70 atsako dažnis buvo stebimas nuo 104 savaitės iki 256 savaitės.
Radiografinis atsakas:
„GO-BEFORE“ tyrimo metu buvo įvertinti vdH-S balo, sudėtinio struktūrinio pažeidimo balo, kuris radiografiškai matuoja sąnarių erozijos skaičių ir dydį bei sąnarių erdvės sumažėjimo laipsnį rankose / riešuose ir pėdose, pokyčiai nuo pradinio lygio. konstrukcijos pažeidimo laipsnis. Pagrindiniai 50 mg Simponi rezultatai 52 savaitę buvo pateikti 3 lentelėje.
Simponi grupėje pacientų, neturinčių naujos erozijos ar bendrojo vdH-S balo pokyčio ≤ 0, skaičius nepasikeitė, buvo žymiai daugiau nei kontrolinėje grupėje (p = 0,003). 52 savaitę pastebėtas radiografinis poveikis išliko iki 104 savaitės. Tarp pacientų, kurie liko tyrime ir buvo gydomi Simponi, radiografinis poveikis buvo panašus nuo 104 iki 256 savaitės.
3 lentelė
Radiografinių pokyčių vidurkis (SD) nuo pradinio iki 52 savaitės bendro vdH-S balo GO-BEFORE tyrimo populiacijoje
a n atitinka atsitiktinių imčių pacientus
* p = 0,015
** p = 0,044
Fizinė funkcija ir su sveikata susijusi gyvenimo kokybė
Fizinė funkcija ir negalia buvo įvertinti kaip atskiros baigtys GO-FORWARD ir GO-AFTER tyrimuose, naudojant HAQ DI neįgalumo indeksą. Šių tyrimų metu 24 savaitę Simponi parodė kliniškai ir statistiškai reikšmingą HAQ DI pagerėjimą, palyginti su pradiniu, palyginti su kontroline grupe. Tarp pacientų, kurie ir toliau vartojo Simponi, atsitiktinių imčių tyrimo pradžioje, HAQ DI pagerėjimas išliko iki 104 savaitės Tarp pacientų, kurie liko tyrime ir buvo gydomi Simponi, HAQ DI pagerėjimas buvo panašus nuo 104 iki 256 savaitės.
GO-FORWARD tyrimo metu klinikiniu ir statistiniu požiūriu reikšmingai pagerėjo su sveikata susijusi gyvenimo kokybė, išmatuota pagal SF-36 fizinių komponentų balą Simponi gydytiems pacientams, palyginti su placebu 24 savaitę. Tarp pacientų, kurie ir toliau vartojo Simponi pradėjus tyrimą, SF-36 pagerėjimas išliko iki 104 savaitės. Tarp pacientų, kurie liko tyrime ir gydomi Simponi, SF-36 fizinio komponento pagerėjimas buvo panašus nuo 104 iki 256 savaitės. „GO-FORWARD“ ir „GO-AFTER“ tyrimai parodė statistiškai reikšmingą nuovargio pagerėjimą, remiantis funkcinio lėtinės ligos terapijos ir nuovargio vertinimo (FACIT-F) skale.
Psoriazinis artritas
Simponi veiksmingumas ir saugumas buvo įvertintas daugiacentriuose, atsitiktinių imčių, dvigubai akluose, placebu kontroliuojamuose klinikiniuose tyrimuose (GO-REVEAL), kuriuose dalyvavo 405 suaugę pacientai, sergantys aktyvia PA (≥ 3 sąnarių patinimas ir ≥ 3 sąnarių skausmas), nepaisant gydymo. su nesteroidiniais vaistais nuo uždegimo (NVNU) arba DMARD. Šio tyrimo pacientai AP diagnozę nustatė mažiausiai 6 mėnesius ir bent jau lengvą psoriazę. Pacientai, sergantys kiekvienu psoriazinio artrito potipiu, įskaitant artritą, buvo įtraukti į poliartritą be reumatoidinio mazgeliai (43%), asimetrinis periferinis artritas (30%), distalinis tarpfalanginio sąnario artritas (DIP) (15%), spondilitas su periferiniu artritu (11%) ir žalojantis artritas (1%). ankstesnio gydymo anti-TNF nebuvo. Simponi arba placebas buvo švirkščiamas po oda kas 4 savaites. Pacientai buvo atsitiktinai suskirstyti į placebą, Simponi 50 mg arba S skirti 100 mg. Pacientai, vartoję placebą, po 24 savaitės buvo paskirti 50 mg Simponi. 52 savaitę pacientai pradėjo ilgalaikį atvirą pratęsimo tyrimą.
Maždaug 48% pacientų toliau vartojo stabilias metotreksato dozes (≤ 25 mg per savaitę). Bendros pirminės baigtys buvo pacientų, kurie 14 savaitę pasiekė atsaką į ACR 20, dalis ir 24 savaitę pasikeitęs bendras AP vdH-S balas nuo pradinio.
Apskritai 104. savaitę nepastebėta kliniškai reikšmingų veiksmingumo rodiklių skirtumų tarp Simponi 50 mg ir 100 mg dozavimo režimų. Remiantis tyrimo planu, ilgą laiką pratęsusiems pacientams gali būti pakeista Simponi 50 mg ir 100 mg dozė. dozes tiriančio gydytojo nuožiūra.
ženklai ir simptomai
Pagrindiniai 50 mg dozės rezultatai 14 ir 24 savaitę pateikti 4 lentelėje ir aprašyti toliau.
4 lentelė
Pagrindiniai GO-REVEAL tyrimo veiksmingumo rezultatai
* p
a n atitinka atsitiktinių imčių pacientus; faktinis pacientų skaičius, kurį galima įvertinti pagal kiekvieną galutinį rezultatą, gali skirtis priklausomai nuo laiko
b Psoriazės plotas ir sunkumo indeksas
c Remiantis pogrupiu pacientų, kurių kūno paviršiaus plotas (BSA) pradžioje buvo ≥ 3%, 79 pacientai (69,9%) placebo grupėje ir 109 (74,3%) 50 mg Simponi.
Atsakymai buvo pastebėti per pirmąjį įvertinimą (4 savaitę) po pirmojo Simponi vartojimo. Panašūs ACR 20 atsakai buvo rasti 14 savaitę pacientams, sergantiems poliartikuliniu artritu, nesant reumatoidinių mazgelių ir AP potipių, asimetrinio periferinio artrito. Kitų PA potipių pacientų skaičius buvo per mažas, kad būtų galima atlikti reikšmingą įvertinimą. Simponi gydymo grupėse pastebėtas atsakas buvo panašus pacientams, gydytiems kartu arba ne kartu su MTX. Iš 146 pacientų, atsitiktinai parinktų 50 mg Simponi, 70 savaitę dar buvo gydomi 104. savaitę. Tarp šių 70 pacientų 64, 46 ir 31 pacientas turėjo atitinkamai 20/50/70 ACR atsaką. Tarp pacientų, kurie liko tyrime ir buvo gydomi Simponi, panašus ACR 20/50/70 atsako dažnis buvo stebimas nuo 104 iki 256 savaitės.
Statistiškai reikšmingas atsakas taip pat buvo pastebėtas DAS28 14 ir 24 savaitę (p
24 savaitę Simponi gydomiems pacientams buvo pastebėtas psoriaziniam artritui būdingų periferinių aktyvumo parametrų pagerėjimas (pvz., Sąnarių patinimas, jautrių sąnarių skaičius, daktilitas ir entezitas). Gydymas Simponi žymiai pagerino fizinę funkciją, kaip nustatyta HAQ DI, ir žymiai pagerino su sveikata susijusią gyvenimo kokybę, remiantis suvestiniais SF-36 fizinių ir psichinių komponentų balais. tyrimo pradžioje DAS28 ir HAQ DI atsakymai išliko iki 104 savaitės. Tarp pacientų, kurie liko tyrime ir buvo gydomi Simponi, DAS28 ir HAQ DI atsakymai buvo panašūs, nuo 104 iki 256 savaitės.
Radiografinis atsakas:
Rankų ir kojų struktūrinė žala buvo radiologiškai įvertinta pagal vdH-S balo pokytį nuo pradinio, modifikuotą AP, pridėjus plaštakos distalinius tarpfalanginius sąnarius (DIP).
Gydymas Simponi 50 mg sumažina periferinių sąnarių pažeidimo progresavimo greitį, palyginti su gydymu placebu 24 savaitę, vertinamas kaip modifikuoto bendro vdH -S balo pokytis nuo pradinio lygio (vidutinis ± SD balas buvo 0,27 ± 1, 3 placebo grupėje, palyginti su - 0,16 ± 1,3 Simponi grupėje; p = 0,011). Iš 146 pacientų, kurie buvo atsitiktinai parinkti 50 mg Simponi, 52 savaitės rentgeno duomenys buvo gauti apie 126 pacientus, iš kurių 77% neparodė progresavimo nuo pradinio lygio. 104 savaitę buvo gauti 114 pacientų rentgeno duomenys, o 77% neparodė progresavimo nuo pradinio lygio. Tarp pacientų, kurie liko tyrime ir buvo gydomi Simponi, panaši dalis pacientų neparodė progresavimo nuo pradinio lygio nuo 104 iki 256 savaitės.
Ašinis spondiloartritas
Ankilozuojantis spondilitas
Simponi veiksmingumas ir saugumas buvo įvertintas daugiacentriuose, dvigubai akluose, atsitiktinių imčių, placebu kontroliuojamuose klinikiniuose tyrimuose (GO-RAISE), kuriuose dalyvavo 356 suaugę pacientai, sergantys aktyviu ankiloziniu spondilitu (apibrėžiamas kaip ankilozinio spondilito patologinis vonios indekso aktyvumas) (BASDAI). ) ≥ 4 ir VAS bendram nugaros skausmui ≥ 4 skalėje nuo 0 iki 10 cm). Į šį tyrimą įtraukti pacientai sirgo liga aktyvioje fazėje, nepaisant dabartinio ar ankstesnio gydymo NVNU ar DMARD, ir anksčiau nebuvo gydomi jokiais anti-TNF vaistais. Simponi arba placebas buvo švirkščiamas po oda kas 4 savaites. Pacientai buvo atsitiktinai suskirstyti į placebą, Simponi 50 mg arba Simponi 100 mg ir galėjo tęsti kartu gydymą DMARD (MTX, SSZ ir (arba) HCQ). Pirminė vertinamoji baigtis buvo pacientų, kuriems buvo diagnozuotas ankilozinio spondilito tyrimo grupės (ASAS 20) atsakas, procentinė dalis 14 savaitę. Placebu kontroliuojami veiksmingumo duomenys buvo renkami ir analizuojami 24 savaitę.
Pagrindiniai 50 mg dozės rezultatai pateikti 5 lentelėje ir aprašyti toliau. Apskritai iki 24 savaitės kliniškai reikšmingų veiksmingumo rodiklių skirtumų tarp Simponi 50 mg ir 100 mg dozavimo režimų nepastebėta. Remiantis tyrimo planu, ilgalaikio pratęsimo pacientams gali būti pakeista Simponi 50 mg ir 100 mg dozė. dozes tiriančio gydytojo nuožiūra.
5 lentelė
Pagrindiniai GO-RAISE tyrimo veiksmingumo rezultatai
* p ≤ 0,001 visiems palyginimams
a n atitinka atsitiktinių imčių pacientus; faktinis pacientų skaičius, kurį galima įvertinti pagal kiekvieną galutinį rezultatą, gali skirtis priklausomai nuo laiko
Tarp pacientų, kurie liko tyrime ir buvo gydomi Simponi, ASAS 20 ir ASAS 40 atsako pacientų dalis buvo panaši nuo 24 iki 256 savaitės.
Statistiškai reikšmingas atsakas taip pat buvo pastebėtas BASDAI 50, 70 ir 90 (p ≤ 0,017) 14 ir 24 savaitę. Pagrindinio ligos aktyvumo matavimų pagerėjimas buvo nustatytas per pirmąjį įvertinimą (4 savaitę) po pradinio Simponi vartojimo, kuris išliko visą savaitę 24. Tyrime dalyvavusių ir Simponi gydytų pacientų BASDAI pokyčiai nuo 24 iki 256 savaitės buvo panašūs.Pacientams, nepriklausomai nuo DMARD vartojimo (MTX, sulfasalazino ir (arba) hidroksichlorokvino), HLA-B27 antigeno buvimo ar pradinio CRP lygio, buvo stebimas nuoseklus veiksmingumas, remiantis 14 savaitės ASAS 20 atsakų įvertinimu.
Gydymas Simponi žymiai pagerino fizinę funkciją, įvertinus 14 ir 24 savaičių pokyčius, palyginti su pradiniu vonios ankilozinio spondilito funkciniu indeksu (BASFI). Su sveikata susijusi gyvenimo kokybė, matuojama pagal sudedamųjų dalių balą. SF-36 pagerėjo 14 ir 24 savaitę. Tarp pacientų, kurie liko tyrime ir gydomi Simponi, fizinės funkcijos ir su sveikata susijusios gyvenimo kokybės pagerėjimas buvo panašus nuo 24 iki 256 savaitės.
Neradiografinis ašinis spondiloartritas
Simponi saugumas ir veiksmingumas buvo įvertintas daugiacentriuose, atsitiktinių imčių, dvigubai akluose, placebu kontroliuojamuose tyrimuose (GO-AHEAD), kuriuose dalyvavo 197 suaugę pacientai, sergantys sunkiu ašiniu SpA Nr. ašinio spondiloartrito diagnozavimo kriterijus, bet neatitiko modifikuotų Niujorko AS diagnozės kriterijų.) Į šį tyrimą įtraukti pacientai sirgo aktyvia liga (nustatyta pagal BASDAI ≥ 4 ir Visual Analogue Scale (VAS) dėl bendro nugaros skausmo). ≥ 4, kiekvienas skalėje nuo 0 iki 10 cm), nepaisant vykstančio ar ankstesnio gydymo NVNU ir anksčiau nebuvo gydytas jokiu biologiniu agentu, įskaitant anti -TNF. 16 savaitę pacientai atvyko atviras gydymo laikotarpis, kurio metu visi vartojo 50 mg Simponi po oda kas 4 savaites iki 48 savaitės, o veiksmingumas buvo vertinamas iki 52 savaitės, o saugumas-iki 60 savaitės. Maždaug 93% pacientų, kurie Simponi vartojo gydymo pradžioje atviras pratęsimas (16 savaitė) buvo gydomas iki tyrimo pabaigos (52 savaitė). Analizė buvo atlikta tiek visai gydomai populiacijai (AT, N = 197), tiek populiacijai, turinčiai objektyvių uždegimo požymių (OSI, N = 158, kaip rodo didelis CRP lygis ir (arba) „sakroilito požymiai MRT Placebo kontroliuojami veiksmingumo duomenys buvo renkami ir analizuojami iki 16 savaitės. Pirminė vertinamoji baigtis buvo pacientų, kurie 16 savaitę pasiekė ASAS 20 atsaką, dalis. Pagrindiniai rezultatai pateikti 6 lentelėje ir aprašyti žemiau.
6 lentelė
Pagrindiniai 16 savaitės GO-AHEAD tyrimo veiksmingumo rezultatai
a n atitinka atsitiktinių imčių ir gydytus pacientus
b Ankilozuojančio spondilito C reaktyviųjų baltymų ligos aktyvumo balas (AT-Placebas, N = 90; AT-Simponi 50 mg, N = 88; OSI-Placebas, N = 71; OSI-Simponi 50 mg, N = 71)
c n atitinka pacientų, kurių pradiniai ir 16 savaitės MRT duomenys, skaičių
d SPARCC (Kanados spondiloartrito tyrimų konsorciumas)
** p prieš placebą
* p prieš placebą
Statistiškai reikšmingai pagerėjo sunkios aktyviosios fazės ašinio SpA požymiai ir simptomai pacientams, gydytiems 50 mg Simponi, palyginti su placebu 16 savaitę (6 lentelė). Pagerėjimas buvo pastebėtas per pirmąjį įvertinimą (4 savaitę) po pirminio Simponi vartojimo. SPARCC MRT rezultatas parodė statistiškai reikšmingą SI sąnario uždegimo sumažėjimą 16 savaitę pacientams, gydytiems 50 mg Simponi, palyginti su placebu (6 lentelė). Skausmas, įvertintas pagal bendrą VAS nugaros skausmą, naktinis nugaros skausmas ir ligos aktyvumas, išmatuotas pagal ASDAS-C, taip pat parodė statistiškai reikšmingą pagerėjimą nuo pradinio lygio iki 16 savaitės pacientams, gydytiems 50 mg Simponi, palyginti su placebu (p
Statistiškai reikšmingas stuburo judrumo pagerėjimas, įvertintas pagal BASMI (vonios ankilozinio spondilito metrologijos indeksą), ir fizinės funkcijos, įvertintos BASFI, buvo nustatytas pacientams, gydytiems Simponi 50 mg, palyginti su pacientais, gydytais placebu (p
Visų pirmiau aprašytų galutinių rodiklių statistiškai reikšmingi rezultatai taip pat buvo parodyti OSI populiacijoje 16 savaitę.
Tiek AT, tiek OSI populiacijose požymių ir simptomų, stuburo judrumo, fizinės funkcijos, gyvenimo kokybės ir produktyvumo pagerėjimas, pastebėtas 16 savaitę tarp pacientų, gydytų Simponi 50 mg, išliko tiems pacientams, kurie liko tyrime. 52 savaitę.
Opinis kolitas
Simponi veiksmingumas buvo įvertintas dviejuose atsitiktinių imčių, dvigubai akluose, placebu kontroliuojamuose klinikiniuose tyrimuose su suaugusiais pacientais.
Įvadinis tyrimas (PURSUIT-Induction) įvertino pacientus, sergančius vidutinio sunkumo ar sunkiu aktyviu opiniu kolitu (Mayo balas nuo 6 iki 12; endoskopinis subvertinimas ≥ 2), kurių atsakas buvo nepakankamas arba kurie netoleravo įprastinio gydymo arba buvo priklausomi nuo kortikosteroidų. Tyrimo dozės patvirtinimo dalyje 761 pacientas buvo atsitiktinai suskirstytas į grupę: 400 mg Simponi SC 0 savaitę ir 200 mg 2 savaitę, Simponi SC 200 mg 0 savaitę ir 100 mg 2 savaitę arba placebo SC 0 savaitę ir 2. Buvo leidžiama kartu vartoti stabilias geriamųjų aminosalicilatų, kortikosteroidų ir (arba) imunomoduliuojančių medžiagų dozes. Šiame tyrime buvo įvertintas Simponi veiksmingumas iki 6 savaitės.
Palaikomojo tyrimo (PURSUIT-Maintenance) rezultatai buvo pagrįsti 456 pacientų, pasiekusių klinikinį atsaką ankstesnės Simponi indukcijos metu, įvertinimu. Pacientai buvo atsitiktinai parinkti, kad kas 4 savaites būtų skiriama 50 mg Simponi, 100 mg Simponi arba placebo. Buvo leidžiama kartu vartoti stabilias geriamųjų aminosalicilatų ir (arba) imunomoduliacinių preparatų dozes. Pradėjus palaikomąjį tyrimą, kortikosteroidai turėjo būti palaipsniui mažinami. Šio tyrimo metu Simponi veiksmingumas buvo įvertintas iki 54 savaitės. Palaikomąjį tyrimą iki 54 savaitės baigę pacientai viename tyrime tęsė gydymą. Pratęsimas, įvertintas veiksmingumas iki 216. savaitės. Veiksmingumo pratęsimo tyrime buvo remiamasi kortikosteroidų vartojimo pokyčiais, gydytojo visuotiniu ligos aktyvumo įvertinimu (PGA) ir gyvenimo kokybės pagerėjimu, išmatuotu pagal uždegiminių žarnų ligų klausimyną (IBDQ).
7 lentelė
Pagrindiniai veiksmingumo rezultatai, gauti iš PURSUIT - indukcijos ir PURSUIT - palaikomųjų tyrimų
N = pacientų skaičius
** p ≤ 0,001
* p ≤ 0,01
a Apibrėžiamas kaip Mayo balo sumažėjimas ≥ 30% ir ≥ 3 taškai, palyginti su pradiniu, kartu su sumažėjusiu kraujavimu iš tiesiosios žarnos sub-balu ≥ 1 arba tiesiosios žarnos kraujavimo sub-balu 0 arba 1.
b Apibrėžiama kaip Mayo rezultatas ≤ 2 taškai, be atskirų sub-balų> 1
c Apibrėžtas kaip 0 arba 1 endoskopiniame Mayo balo balo rezultate.
d Indukcija tik naudojant Simponi.
e Pacientai buvo vertinami pagal CU aktyvumą pagal Mayo dalinį balą kas 4 savaites (atsako praradimas buvo patvirtintas atliekant endoskopiją). Todėl vienas pacientas, kuris išlaikė atsaką, buvo nuolatinis klinikinis atsakas kiekvieno klinikinio įvertinimo metu iki 54 savaitės.
f 30–54 savaites pacientas turėjo būti remisijos stadijoje (iki 54 savaitės atsakas neteko), kad pasiektų ilgalaikę remisiją.
g Pacientams, sveriantiems mažiau nei 80 kg, didesnė dalis pacientų, kuriems buvo taikoma 50 mg palaikomoji terapija, turėjo ilgalaikę klinikinę remisiją nei tie, kurie vartojo placebą.
Daugiau Simponi gydytų pacientų gleivinės gijimas buvo ilgalaikis (pacientai gleivinės išgydė 30 ir 54 savaites) 50 mg grupėje (42%, nominalus p
Tarp 54% pacientų (247/456), kurie PURSUIT-Maintenance pradžioje buvo gydomi kartu su kortikosteroidais, pacientų, kurie išlaikė klinikinį atsaką iki 54 savaitės ir kurie kartu su kortikosteroidais gydymo pradžioje negavo, dalis 54 savaitė buvo didesnė 50 mg grupėje (38%, 30/78) ir 100 mg grupėje (30%, 25/82), palyginti su placebo grupe (21%, 18/87). kurie iki 54 savaitės pašalino kortikosteroidus, buvo didesni 50 mg grupėje (41%, 32/78) ir 100 mg grupėje (33%, 27/82), palyginti su placebo grupe (22%, 19/87). buvo įtrauktas į pratęsimo tyrimą, tiriamųjų, kurie liko be kortikosteroidų, dalis paprastai išliko iki 216 savaitės.
6 savaitę Simponi žymiai pagerino gyvenimo kokybę, matuojant pokyčius, lyginant su pradiniais rodikliais, taikant konkrečiai ligai skirtą priemonę-IBDQ (uždegiminių žarnų ligų klausimyną). Tarp pacientų, kuriems buvo taikomas palaikomasis gydymas Simponi, gyvenimo kokybės pagerėjimas, išmatuotas pagal IBDQ buvo išlaikytas iki 54 savaitės.
Maždaug 63% pacientų, kurie Simponi vartojo pratęsimo tyrimo pradžioje (56 savaitę), gydėsi iki tyrimo pabaigos (paskutinis golimumabo vartojimas 212 savaitę).
Imunogeniškumas
III fazės RA, AP ir SA tyrimuose iki 52 savaitės 5% (105/2062) golimumabu gydytų pacientų buvo aptikti antikūnai prieš golimumabą, naudojant imuninį fermentinį tyrimą (PAV), ir kai buvo tirti, beveik visi buvo neutralizuojantys antikūnai in vitro. Panašūs procentai buvo nurodyti reumatologinėse indikacijose. Kartu vartojant MTX, pacientų, turinčių antikūnų prieš golimumabą, procentas buvo mažesnis nei pacientų, kurie vartojo golimumabą be MTX (atitinkamai maždaug 3% [41/1235], palyginti su 8% [64/827]).
Atliekant PIA tyrimą, ašinis SpA nr, antikūnai prieš golimumabą buvo aptikti 7% (14/193) golimumabu gydytų pacientų.
II ir III fazės UC tyrimuose iki 54 savaitės, atliekant PAV tyrimą, 3% (26/946) golimumabu gydytų pacientų buvo aptikta antikūnų prieš golimumabą. Šešiasdešimt aštuoni procentai (21/31) antikūnų teigiamų pacientų turėjo neutralizuojančių antikūnų in vitro. Kartu vartojant imunomoduliatorius (azatiopriną, 6-merkaptopuriną ir MTX), pacientų, turinčių antikūnų prieš golimumabą, dalis buvo mažesnė nei pacientų, vartojusių golimumabą be imunomoduliatorių (atitinkamai 1% (4/308), palyginti su 3% (22). / 638)). Tarp pacientų, kurie tęsė pratęsimo tyrimą ir kurių mėginiai buvo įvertinti iki 228 savaitės, antikūnų prieš golimumabą buvo aptikta 4% (23/604) golimumabu gydytų pacientų. 82 procentai (18/22) pacientų, kuriems buvo nustatyti antikūnai, turėjo neutralizuojančių antikūnų in vitro.
PIA tyrime, siekiant nustatyti antikūnus prieš golimumabą, buvo naudojamas vaistams toleruojamas PAV tyrimas. Atsižvelgiant į padidėjusį jautrumą ir geresnę vaistų toleranciją, tikimasi, kad atliekant PAV tyrimą bus nustatytas didesnis antikūnų prieš golimumabą dažnis. lyginant su PAV. III fazės PIA tyrime iki 48 savaitės antikūnai prieš golimumabą buvo nustatyti vaistams toleruojant PAV tyrimą 40% (69/172) golimumabu gydytų vaikų, kurių daugumos titras buvo mažesnis nei 1: 1 000. Poveikis golimumabo koncentracijai serume buvo pastebėtas, kai titrai> 1: 100, o poveikio titrui> 1: 1000, tačiau vaikų, kurių titrai> 1: 1000, buvo nedaug (N = 8). Tarp vaikų, kurių golimumabo antikūnai buvo teigiami, 39% (25/65) turėjo neutralizuojančių antikūnų. Didesnis antikūnų dažnis atliekant vaistą toleruojantį PAV tyrimą, atsižvelgiant į tai, kad tai daugiausia buvo mažo titro antikūnai, neturėjo akivaizdžios įtakos vaistų lygiui, veiksmingumui ir saugumui, todėl nepateikia jokių naujų saugumo signalų.
Jei antikūnų prieš golimumabą gali padidėti reakcijos injekcijos vietoje rizika (žr. 4.4 skyrių). Nedidelis golimumabo antikūnų teigiamų pacientų skaičius riboja galimybę daryti tvirtas išvadas dėl ryšio tarp anti-golimumabo antikūnų ir klinikinio veiksmingumo ar saugumo priemonių.
Kadangi imunogeniškumo tyrimai yra specifiniai konkrečiam produktui ir tyrimui, antikūnų procentinės dalies palyginimas su kitų produktų kiekiu yra netinkamas.
Vaikų populiacija
Jaunatvinis idiopatinis poliartritinis artritas
Simponi saugumas ir veiksmingumas buvo įvertintas atsitiktinių imčių, dvigubai aklu, placebu kontroliuojamu suspensijos tyrimu (GO-KIDS), kuriame dalyvavo 173 vaikai (nuo 2 iki 17 metų), turintys aktyvią pJIA, turintys bent 5 aktyvius sąnarius ir nepakankami. atsakas į MTX. Į tyrimą buvo įtraukti vaikai, sergantys poliartikuline JIA eiga (reumatoidiniu faktoriumi teigiamas arba neigiamas poliartritas, platus oligoartritas, jaunatvinis psoriazinis artritas arba sisteminis JIA, neturintis nuolatinių sisteminių simptomų). Vidutinis aktyvių sąnarių skaičius iš pradžių buvo 12 ir vidutinis CRP buvo 0,17 mg / dL.
1 tyrimo dalis apėmė atvirą 16 savaičių fazę, kurioje 173 įtraukti vaikai gavo Simponi 30 mg / m2 (ne daugiau kaip 50 mg) po oda kas 4 savaites ir MTX. 154 vaikai, pasiekę ACR Ped 30 atsaką 16 savaitę, pateko į 2 tyrimo dalį, atsitiktinės atrankos fazę ir gavo Simponi po 30 mg / m2 (ne daugiau kaip 50 mg) + MTX arba placebą + MTX. Po ligos paūmėjimo vaikai gavo Simponi 30 mg / m2 (daugiausia 50 mg) + MTX. 48 savaitę kūdikiai pateko į ilgalaikį pratęsimo etapą.
Šio tyrimo vaikai ACR Ped 30, 50, 70 ir 90 atsakymus parodė jau 4 savaitę.
16 savaitę 87% vaikų atsakė į ACR Ped 30 ir 79%, 66% ir 36% vaikų buvo atitinkamai ACR Ped 50, ACR Ped 70 ir ACR Ped 90. 16 savaitę 34 % vaikų sirgo neaktyvia liga, kurią apibūdina visi šie veiksniai: sąnarių nebuvimas su aktyviu artritu; karščiavimo, bėrimo, serozito, splenomegalijos, hepatomegalijos ar generalizuotos limfadenopatijos nebuvimas, susijęs su JIA; aktyvaus uveito nebuvimas; normalus ESR (
16 savaitę visi ACR Ped komponentai parodė kliniškai reikšmingą pagerėjimą, palyginti su pradiniu (žr. 8 lentelę).
8 lentelė
ACR Ped komponentų patobulinimai 16 savaitę
pradžioje = 0 savaitė
b „n“ atspindi įtrauktus pacientus
c VAS: vizualinė analoginė skalė
d CHAQ: Vaikų sveikatos vertinimo klausimynas
ir ESR (mm / h): eritrocitų nusėdimo greitis (milimetrais per valandą)
Pagrindinė tyrimo baigtis - vaikų, kuriems buvo atsakas į ACR Ped 30, procentas 16 savaitę ir kuriems nebuvo paūmėjimo tarp 16 ir 48 savaičių. 16 ir 48 savaitės (59% Simponi + MTX grupėje ir 53% placebo + MTX grupėje; p = 0,41).
Iš anksto nustatyta pirminės vertinamosios baigties pogrupio analizė, pagrįsta pradinėmis CRP reikšmėmis (≥ 1 mg / dL vs.
48 savaitę 53% ir 55% Simponi + MTX ir placebo + MTX grupės vaikų buvo ACR Ped 30 atsakas, o 40% ir 28% vaikų Simponi + MTX grupėje ir placebas + MTX atitinkamai pasiekė neaktyvią ligą.
Europos vaistų agentūra atidėjo įpareigojimą pateikti Simponi tyrimų rezultatus vaikams, sergantiems opiniu kolitu (informaciją apie vartojimą vaikams žr. 4.2 skyriuje).
05.2 Farmakokinetinės savybės
Absorbcija
Vieną kartą po oda sušvirkštus golimumabo sveikiems asmenims ar RA sergantiems pacientams, vidutinis laikas iki didžiausios koncentracijos serume (Tmax) buvo nuo 2 iki 6 dienų.Sveikiems asmenims po oda sušvirkštus 50 mg golimumabo, vidutinė ± standartinio nuokrypio didžiausia koncentracija serume (Cmax) buvo 3,1 ± 1,4 μg / ml.
Po vienos 100 mg injekcijos po oda golimumabo absorbcija rankoje, pilve ir šlaunyje buvo panaši, vidutinis absoliutus biologinis prieinamumas - 51%. Po oda absoliutus 50 mg arba 200 mg golimumabo dozės biologinis prieinamumas turėtų būti panašus.
Paskirstymas
Po vienkartinės IV injekcijos vidutinis pasiskirstymo tūris buvo 115 ± 19 ml / kg.
Eliminavimas
Sisteminis golimumabo klirensas buvo 6,9 ± 2,0 ml per parą / kg. Apskaičiuota, kad galutinis pusinės eliminacijos laikas sveikiems asmenims yra maždaug 12 ± 3 dienos, o pacientų, sergančių RA, AP, SA ar CU, vertės buvo panašios.
Kai RA, AP ar AS sergantiems pacientams po oda buvo švirkščiama 50 mg golimumabo dozė kas 4 savaites, koncentracija serume pasiekė pastovią būseną iki 12 savaitės. Kartu vartojant MTX, 50 mg golimumabo po oda kas 4 savaites (± standartinis nuokrypis) mažiausia koncentracija serume esant pastoviai maždaug 0,6 ± 0,4 μg / ml pacientams, sergantiems aktyviu RA, nepaisant gydymo MTX, maždaug 0,5 ± 0,4 μg / ml pacientams, sergantiems aktyviu PA, ir maždaug 0,8 ± 0,4 μg / ml Pacientai, sergantys AS: Golimumabo vidutinė pusiausvyrinė koncentracija serume pacientams, sergantiems ašiniu SpA nr, buvo panaši į tą, kuri buvo pastebėta AS pacientams, po oda švirkščiant 50 mg golimumabo kas 4 savaites.
Pacientams, sergantiems RA, AP ar SA, kurie kartu neskyrė MTX, buvo maždaug 30% mažesnė golimumabo pusiausvyros koncentracijos koncentracija nei pacientų, vartojusių golimumabą kartu su MTX. Ribotam skaičiui RA pacientų, gydytų golimumabu po oda ilgiau nei 6 mėnesius, kartu vartojant MTX, akivaizdus golimumabo klirensas sumažėjo maždaug 36%. Tačiau populiacijos farmakokinetikos analizės rodo, kad kartu vartojami NVNU, geriamieji kortikosteroidai ar sulfasalazinas neturėjo įtakos tariamam golimumabo klirensui.
Po 200 mg ir 100 mg golimumabo dozių atitinkamai 0 ir 2 savaitę, o po to palaikomosiomis 50 mg arba 100 mg golimumabo dozėmis po oda kas 4 savaites UC sergantiems pacientams golimumabo koncentracija serume pasiekė pusiausvyrą maždaug po 14 savaičių nuo gydymo pradžios. Gydant 50 mg arba 100 mg golimumabo po oda kas 4 savaites palaikomojo gydymo metu, vidutinė pusiausvyrinė koncentracija serume buvo maždaug 0,9 ± 0,5 mcg / ml ir 1,8 ± 1,1 mcg / ml.
Pacientams, sergantiems UC, 50 mg arba 100 mg golimumabo po oda kas 4 savaites, kartu vartojant imunomoduliatorius esminės įtakos pusiausvyros golimumabo koncentracijai nebuvo.
Pacientams, kuriems atsirado anti-golimumabo antikūnų, buvo maža mažiausia golimumabo pusiausvyros koncentracijos serume koncentracija (žr. 5.1 skyrių).
Tiesiškumas
Pacientams, sergantiems reumatoidiniu artritu, golimumabo farmakokinetikos parametrai buvo maždaug proporcingi dozei 0,1–10,0 mg / kg dozėje po vienkartinės intraveninės dozės. Sveikiems asmenims pavartojus vienkartinę SC dozę, taip pat buvo stebimi maždaug su doze proporcingi farmakokinetikos parametrai. Nuo 50 mg iki 400 mg.
Svorio įtaka farmakokinetikai
Pastebima tendencija, kad golimumabo klirensas didėja didėjant svoriui (žr. 4.2 skyrių).
Vaikų populiacija
Golimumabo farmakokinetika nustatyta 173 vaikams, sergantiems pJIA nuo 2 iki 17 metų. Atliekant pJIA tyrimą, vaikams, gydomiems po oda 30 mg / m2 (ne daugiau kaip 50 mg) po oda kas 4 savaites, vidutinė pusiausvyrinė golimumabo koncentracija buvo panaši visose amžiaus grupėse ir taip pat buvo panaši arba šiek tiek didesnė nei suaugusiųjų RA pacientų, gydomų 50 mg golimumabu kas 4 savaites.
Populiacijos farmakokinetikos / farmakodinamikos modeliai ir modeliavimas vaikams, sergantiems pJIA, patvirtino ryšį tarp golimumabo ekspozicijos serume ir klinikinio veiksmingumo ir patvirtina, kad 50 mg golimumabo dozavimo režimas vaikams, kurių pJIA sveria ne mažiau kaip 40 kg, leidžia pasiekti ekspoziciją, panašią į tas, kurios buvo įrodyta, kad jie yra veiksmingi suaugusiesiems.
05.3 Ikiklinikinių saugumo duomenys
Įprastų farmakologinio saugumo, kartotinių dozių toksiškumo, toksiškumo reprodukcijai ir vystymosi ikiklinikinių tyrimų duomenys specifinio pavojaus žmogui nerodo.
Mutageniškumo, gyvūnų vaisingumo ar ilgalaikio kancerogeniškumo tyrimų su golimumabu neatlikta.
Atlikus pelių vaisingumo ir bendros reprodukcinės funkcijos tyrimą, naudojant panašų antikūną, kuris selektyviai slopina pelių TNF α funkcinį aktyvumą, nėščių pelių skaičius sumažėjo. Nežinoma, ar šie rezultatai atsirado dėl poveikio patinams ir (arba) Evoliucinio toksiškumo tyrimo, atlikto su pelėmis po to paties analoginio antikūno ir cynomolgus beždžionių, vartojančių golimumabą, metu nebuvo jokių toksiškumo motinai, toksiškumo embrionui ar teratogeniškumo požymių.
06.0 FARMACINĖ INFORMACIJA
06.1 Pagalbinės medžiagos
Sorbitolis (E420)
L-histidinas
L-histidino monohidrochlorido monohidratas
Polisorbatas 80
Injekcinis vanduo.
06.2 Nesuderinamumas
Nesant suderinamumo tyrimų, šio vaistinio preparato negalima maišyti su kitais produktais.
06.3 Galiojimo laikas
22 mėnesiai
06.4 Specialios laikymo sąlygos
Laikyti šaldytuve (2 ° C - 8 ° C).
Negalima užšaldyti.
Užpildytą švirkštiklį arba užpildytą švirkštą laikyti išorinėje dėžutėje, kad preparatas būtų apsaugotas nuo šviesos.
06.5 Pirminės pakuotės pobūdis ir pakuotės turinys
Simponi 50 mg injekcinis tirpalas užpildytoje švirkštimo priemonėje
0,5 ml tirpalo užpildytame švirkšte (1 tipo stiklas) su fiksuota adata (nerūdijantis plienas) ir adatos dangteliu (guma, kurioje yra latekso) užpildytoje švirkštimo priemonėje. Simponi tiekiamas pakuotėmis, kuriose yra 1 užpildytas švirkštas švirkštimo priemonę ir sudėtines pakuotes, kuriose yra 3 užpildytos švirkštimo priemonės (3 pakuotės po 1).
Simponi 50 mg injekcinis tirpalas užpildytame švirkšte
0,5 ml tirpalo užpildytame švirkšte (1 tipo stiklas) su fiksuota adata (nerūdijantis plienas) ir adatos dangteliu (guma, kurioje yra latekso). Simponi tiekiamas pakuotėse po 1 užpildytą švirkštą ir daugybinėse pakuotėse po 3 (3 pakuotės po 1) užpildytus švirkštus.
Gali būti tiekiamos ne visų dydžių pakuotės.
06.6 Naudojimo ir naudojimo instrukcijos
Simponi tiekiamas vienkartiniame užpildytame švirkštiklyje, vadinamame „SmartJect“, arba vienkartiniame užpildytame švirkšte. Kiekvienoje Simponi pakuotėje yra naudojimo instrukcijos, kuriose išsamiai aprašyta, kaip naudoti švirkštiklį ar švirkštą. Išėmus iš šaldytuvo užpildytą švirkštiklį ar užpildytą švirkštą, prieš švirkščiant Simponi, reikia palaukti, kol jis sušils iki kambario temperatūros. Švirkštiklio ar švirkšto negalima purtyti.
Tirpalas yra skaidrus arba šiek tiek opalescuojantis, bespalvis arba šviesiai gelsvas ir gali turėti smulkių permatomų arba baltų baltymų dalelių. Tai nėra neįprasta tirpalams, kurių sudėtyje yra baltymų.
Simponi negalima vartoti, jei tirpalo spalva pasikeitė, jis yra drumstas arba jame yra matomų pašalinių dalelių.
Išsamios Simponi paruošimo ir vartojimo instrukcijos užpildytame švirkštiklyje arba užpildytame švirkšte pateikiamos pakuotės lapelyje.
Nepanaudotą vaistą ir jo atliekas reikia sunaikinti laikantis vietinių taisyklių.
07.0 RINKODAROS TEISĖS TURĖTOJAS
Janssen Biologics B.V.
Einšteinas 101
2333 CB Leidenas
Nyderlandai
08.0 RINKODAROS TEISĖS NUMERIS
EU/1/09/546/001 1 užpildyta švirkštimo priemonė
EU/1/09/546/002 3 užpildytos švirkštimo priemonės
EU/1/09/546/003 1 užpildytas švirkštas
EU/1/09/546/004 3 užpildyti švirkštai
039541014
039541026
039541038
039541040
09.0 RINKODAROS TEISĖS SUTEIKIMO AR PATVIRTINIMO DATA
Registravimo data: 2009 m. Spalio 1 d
Paskutinio atnaujinimo data: 2014 m. Birželio 19 d
10.0 TEKSTO PERŽIŪROS DATA
2017 m. Vasario 02 d
11.0 RADIJO NARKOTIKŲ VISIŠKAI VIDINIO RADIACIJOS Dozimetrijos duomenys
12.0 RADIJO NARKOTIKAI, PAPILDOMOS IŠSAMIOS NURODYMAI APIE LAIKINĄ PARUOŠIMĄ IR KOKYBĖS KONTROLĘ