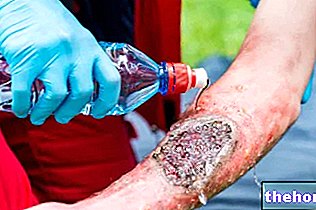
Veikliosios medžiagos: Anidulafunginas
ECALTA 100 mg milteliai koncentratui infuziniam tirpalui
Indikacijos Kodėl vartojamas Ecalta? Kam tai?
ECALTA sudėtyje yra veikliosios medžiagos anidulafungino ir jis vartojamas suaugusiesiems gydyti kraujo ar kitų vidaus organų grybelinę infekciją, vadinamą invazine kandidoze. Infekciją sukelia grybelio (mielių), vadinamo Candida, ląstelės.
ECALTA priklauso vaistų, vadinamų echinokandinais, grupei. Šie vaistai vartojami sunkioms grybelinėms infekcijoms gydyti.
ECALTA apsaugo nuo normalaus grybelinių ląstelių sienelių vystymosi. Esant ECALTA, grybelinės ląstelės turi neišsamias arba pažeistas ląstelių sieneles, todėl jos tampa trapios arba negali augti.
Kontraindikacijos Kada Ecalta vartoti negalima
ECALTA vartoti negalima:
- jeigu yra alergija anidulafunginui, kitiems echinokandinams (pvz., CANCIDAS) arba bet kuriai pagalbinei šio vaisto medžiagai.
Atsargumo priemonės Vartojant prieš vartojant Ecalta
Pasitarkite su gydytoju, vaistininku arba slaugytoja, prieš pradėdami vartoti ECALTA
- atidžiau kepenų funkciją, jei gydymo metu atsiranda kepenų sutrikimų.
- jeigu gydymo ECALTA metu jums duodama anestetikų.
Vaikai
ECALTA negalima skirti jaunesniems nei 18 metų pacientams.
Sąveika Kokie vaistai ar maistas gali pakeisti Ecalta poveikį
Jeigu vartojate arba neseniai vartojote kitų vaistų arba dėl to nesate tikri, apie tai pasakykite gydytojui arba vaistininkui.
Nepradėkite vartoti kitų vaistų ir nenustokite jų vartoti be gydytojo ar vaistininko sutikimo.
Įspėjimai Svarbu žinoti, kad:
Nėštumas ir žindymo laikotarpis
ECALTA poveikis nėščioms moterims nežinomas, todėl nėštumo metu ECALTA vartoti nerekomenduojama. Vaisingos moterys turi naudoti tinkamą kontracepcijos metodą. Nedelsdami kreipkitės į gydytoją, jei gydymo ECALTA metu pastojote.
ECALTA poveikis žindančioms moterims nežinomas. Prieš vartodami pasitarkite su gydytoju arba vaistininku.
ECALTA žindymo laikotarpiu. Prieš vartodami bet kokį vaistą, pasitarkite su gydytoju arba vaistininku.
ECALTA sudėtyje yra fruktozės
Šio vaisto sudėtyje yra fruktozės (tam tikros rūšies cukraus). Jei gydytojas Jums yra sakęs, kad netoleruojate kokių nors angliavandenių, prieš vartodami šį vaistą pasitarkite su gydytoju.
Dozė, vartojimo būdas ir laikas Kaip vartoti Ecalta: Dozavimas
ECALTA visada paruoš ir suleis gydytojas arba sveikatos priežiūros specialistas (daugiau informacijos apie šio vaisto paruošimo būdą rasite pakuotės lapelio pabaigoje, skirtame gydytojams ir sveikatos priežiūros specialistams).
Pirmąją dieną gydymas pradedamas nuo 200 mg (įsotinamoji dozė). Po to bus skiriama 100 mg paros dozė (palaikomoji dozė).
ECALTA Jums leidžiama vieną kartą per parą lėta (lašinama) infuzija į veną. Palaikomoji dozė užtruks mažiausiai 1,5 valandos, o įsotinamoji - 3 valandas.
Gydytojas nustatys gydymo trukmę ir ECALTA kiekį, kurį gausite kiekvieną dieną, ir patikrins jūsų atsaką į gydymą bei jūsų būklę.
Apskritai gydymas turi būti tęsiamas mažiausiai 14 dienų nuo paskutinės Candida aptikimo kraujyje dienos.
Pamiršus pavartoti ECALTA
Kadangi šis vaistas jums bus skiriamas atidžiai prižiūrint gydytojui, mažai tikėtina, kad dozė bus praleista. Tačiau pasakykite gydytojui arba vaistininkui, jei manote, kad dozė buvo praleista.
Gydytojas neturėtų duoti dvigubos dozės.
Nustojus vartoti ECALTA
Jei gydytojas nustoja vartoti ECALTA, poveikis neturėtų būti.
Gydytojas gali paskirti kitą vaistą po gydymo ECALTA, kad tęstų grybelinės infekcijos gydymą arba neleistų jai atsinaujinti.
Jei pirminiai infekcijos simptomai kartojasi, nedelsdami pasakykite gydytojui arba kitam sveikatos priežiūros specialistui.
Jeigu kiltų daugiau klausimų dėl šio vaisto vartojimo, kreipkitės į gydytoją, vaistininką arba slaugytoją.
Paruošimas
Kiekvieną buteliuką reikia aseptinėmis sąlygomis ištirpinti 30 ml injekcinio vandens, kad būtų pasiekta 3,33 mg / ml koncentracija. Paruošimo laikas gali trukti iki 5 minučių. Po to praskiedimo tirpalą reikia išmesti, jei yra dalelių arba pakitusi spalva.
Paruoštą tirpalą iki kito praskiedimo galima laikyti iki 25 ° C iki 24 valandų.
Skiedimas ir infuzija
Paruoštą buteliuko turinį aseptinėmis sąlygomis reikia perkelti į intraveninį maišelį (arba buteliuką), kuriame yra 9 mg / ml (0,9%) infuzinio natrio chlorido arba 50 mg / ml (5%) infuzinės gliukozės. anidulafungino koncentracija lygi 0,77 mg / ml. Žemiau esančioje lentelėje parodytas kiekvienai dozei reikalingas tūris.
Skiedimo reikalavimai vartojant ECALTA
A: natrio chloridas infuzijai 9 mg / ml (0,9%) arba gliukozė infuzijai 50 mg / ml (5%)
B: Infuzinio tirpalo koncentracija yra 0,77 mg / ml. Infuzijos greitis neturi viršyti 1,1 mg / min (atitinka 1,4 ml / min., Ištirpinus ir praskiedus, kaip nurodyta).
Kai tik leidžia tirpalas ir talpykla, prieš vartojant parenteralinius vaistinius preparatus reikia vizualiai apžiūrėti, ar nėra dalelių ar spalvos pakitimų.
Tik vienkartiniam naudojimui. Nepanaudotą vaistą ir jo atliekas reikia sunaikinti laikantis vietinių taisyklių.
Perdozavimas Ką daryti pavartojus per didelę Ecalta dozę
Jei nerimaujate, kad jums galėjo būti suleista daugiau ECALTA nei reikia, nedelsdami pasakykite gydytojui arba kitam sveikatos priežiūros specialistui.
Šalutinis poveikis Koks yra Ecalta šalutinis poveikis
Šis vaistas, kaip ir visi kiti, gali sukelti šalutinį poveikį, nors jis pasireiškia ne visiems žmonėms. Kai kuriuos iš šių šalutinių poveikių pastebės gydytojas, stebėdamas jūsų atsaką ir būklę.
Vartojant ECALTA, retai buvo pranešta apie gyvybei pavojingas alergines reakcijas, įskaitant pasunkėjusį kvėpavimą, švokštimą ar pasunkėjusį išbėrimą.
Sunkus šalutinis poveikis - nedelsdami pasakykite gydytojui arba kitam sveikatos priežiūros specialistui, jei pasireiškė kuris nors iš šių reiškinių:
- Traukuliai (traukuliai)
- Paraudimas
- Odos bėrimas, niežulys
- Karščio bangos
- Dilgėlinė
- Staigus kvėpavimo takų raumenų susitraukimas, galintis sukelti švokštimą ar kosulį
- Sunkumas kvėpuoti
Kitas šalutinis poveikis
Labai dažnas šalutinis poveikis (gali pasireikšti daugiau kaip 1 iš 10 žmonių) yra:
- Mažas kalio kiekis kraujyje (hipokalemija)
- Viduriavimas
- Pykinimas
Dažnas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 10 žmonių) yra:
- Traukuliai (traukuliai)
- Galvos skausmas
- Jis atsitraukė
- Kepenų funkcijos tyrimų pokyčiai
- Odos bėrimas, niežulys
- Inkstų funkcijos tyrimų pokyčiai
- Tulžies srauto iš tulžies pūslės į žarnyną keitimas (cholestazė)
- Aukštas cukraus kiekis kraujyje
- Aukštas kraujo spaudimas
- Žemas kraujo spaudimas
- Staigus kvėpavimo takų raumenų susitraukimas, galintis sukelti švokštimą ar kosulį
- Sunkumas kvėpuoti
Nedažnas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių) yra:
- Krešėjimo sutrikimai
- Paraudimas
- Karščio bangos
- Pilvo skausmas
- Dilgėlinė
- Skausmas injekcijos vietoje
Nepageidaujamas poveikis, kurio dažnis nežinomas (dažnis negali būti įvertintas pagal turimus duomenis):
- Alerginės reakcijos, keliančios grėsmę gyvybei
Pranešimas apie šalutinį poveikį
Jeigu pasireiškė šalutinis poveikis (net jeigu jis šiame lapelyje nenurodytas), kreipkitės į gydytoją, vaistininką arba slaugytoją. Apie šalutinį poveikį taip pat galite pranešti tiesiogiai naudodamiesi V pranešimo sistema. Pranešdami apie šalutinį poveikį galite padėti. suteikti daugiau informacijos apie šio vaisto saugumą.
Galiojimo laikas ir išlaikymas
Šį vaistą laikykite vaikams nepastebimoje ir nepasiekiamoje vietoje. Ant etiketės nurodytam tinkamumo laikui pasibaigus, šio vaisto vartoti negalima. Vaistas tinkamas vartoti iki paskutinės nurodyto mėnesio dienos.
Laikyti šaldytuve (2 ° C - 8 ° C).
Paruoštą tirpalą galima laikyti iki 25 ° C temperatūroje iki 24 valandų. Infuzinį tirpalą galima laikyti ne aukštesnėje kaip 48 valandų temperatūroje 25 ° C temperatūroje (kambario temperatūroje) arba mažiausiai 72 valandas užšaldyti, o per 48 valandas jis turi būti suleistas 25 ° C temperatūroje (kambario temperatūroje).
Neišmeskite jokių vaistų į kanalizaciją ar buitines atliekas.
Kita informacija
ECALTA sudėtis
Veiklioji medžiaga yra anidulafunginas. Kiekviename miltelių buteliuke yra 100 mg anidulafungino
Pagalbinės medžiagos yra fruktozė, manitolis, polisorbatas 80, vyno rūgštis, natrio hidroksidas (pH koreguoti), druskos rūgštis (pH koreguoti).
ECALTA išvaizda ir kiekis pakuotėje
ECALTA tiekiamas pakuotėje, kurioje yra 1 buteliukas su 100 mg miltelių koncentratui infuziniam tirpalui.
Milteliai yra balti arba beveik balti.
Šaltinio pakuotės lapelis: AIFA (Italijos vaistų agentūra). Turinys paskelbtas 2016 m. Sausio mėn. Pateikta informacija gali būti neatnaujinta.
Norint pasiekti naujausią versiją, patartina apsilankyti AIFA (Italijos vaistų agentūra) svetainėje. Atsisakymas ir naudinga informacija.
01.0 VAISTINIO PREPARATO PAVADINIMAS
ECALTA 100 MG milteliai infuzinio tirpalo koncentratui
02.0 KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
Kiekviename buteliuke yra 100 mg anidulafungino.
Paruoštame tirpale yra 3,33 mg / ml anidulafungino, o praskiestame - 0,77 mg / ml anidulafungino.
Pagalbinė medžiaga, kurios poveikis žinomas102.5 mg fruktozės buteliuke.
Išsamų pagalbinių medžiagų sąrašą žr. 6.1 skyriuje.
03.0 FARMACINĖ FORMA
Milteliai infuzinio tirpalo koncentratui.
Baltas arba beveik baltas kietas liofilizatas.
Paruošto tirpalo pH yra 3,5–5,5.
04.0 KLINIKINĖ INFORMACIJA
04.1 Terapinės indikacijos
Suaugusių pacientų invazinės kandidozės gydymas (žr. 4.4 ir 5.1 skyrius).
04.2 Dozavimas ir vartojimo metodas
Gydymą ECALTA turi pradėti gydytojas, turintis invazinių grybelinių infekcijų gydymo patirties. Prieš pradedant gydymą, reikia surinkti grybelių kultūrų mėginius. Gydymą galima pradėti prieš žinant pasėlių tyrimų rezultatus ir juos atitinkamai pritaikyti, kai šie rezultatai bus žinomi.
Dozavimas
Pirmąją gydymo dieną reikia skirti vieną 200 mg įsotinamąją dozę, vėliau - 100 mg per parą. Gydymo trukmė turi būti pagrįsta klinikiniu paciento atsaku. Paprastai priešgrybelinis gydymas turi būti tęsiamas mažiausiai 14 dienų po paskutinės teigiamos kultūros.
Trukmė gydymo
Nėra pakankamai duomenų, kad būtų galima pagrįsti 100 mg dozės vartojimą ilgiau nei 35 dienas.
Pacientai, kurių inkstų ir kepenų funkcija sutrikusi
Pacientams, kuriems yra lengvas, vidutinio sunkumo ar sunkus kepenų funkcijos sutrikimas, dozės koreguoti nereikia. Pacientams, kuriems yra bet kokio laipsnio inkstų funkcijos sutrikimas, įskaitant pacientus, kuriems atliekama dializė, dozės koreguoti nereikia. ECALTA galima vartoti nepriklausomai nuo to, kada atliekama dializė (žr. 5.2 skyrių).
Kitos specialios pacientų grupės
Suaugusiems pacientams dozės keisti nereikia, atsižvelgiant į lytį, svorį, etninę kilmę, ŽIV pozityvumą arba senyvo amžiaus pacientams (žr. 5.2 skyrių).
Vaikų populiacija
ECALTA saugumas ir veiksmingumas jaunesniems kaip 18 metų vaikams nenustatytas.Šiuo metu turimi duomenys aprašyti 5.2 skyriuje, tačiau neįmanoma nustatyti rekomenduojamo režimo.
Vartojimo metodas
Tik intraveniniam vartojimui.
ECALTA reikia ištirpinti 3,33 mg / ml koncentracijos injekciniu vandeniu, o po to praskiesti iki 0,77 mg / ml koncentracijos. Instrukcijos, kaip paruošti vaistinį preparatą prieš vartojimą, pateikiamos 6.6 skyriuje.
Rekomenduojama ECALTA vartoti infuzijos greičiu, kuris neviršija 1,1 mg / min (atitinka 1,4 ml / min., Kai milteliai ištirpinami ir praskiedžiami taip, kaip nurodyta). Su infuzija susijusios reakcijos yra retos, kai anidulafungino infuzijos greitis neviršija 1,1 mg / min (žr. 4.4 skyrių).
ECALTA negalima švirkšti kaip boliuso.
04.3 Kontraindikacijos
Padidėjęs jautrumas veikliajai arba bet kuriai 6.1 skyriuje nurodytai pagalbinei medžiagai.
Padidėjęs jautrumas kitiems echinokandinų klasės vaistams.
04.4 Specialūs įspėjimai ir tinkamos atsargumo priemonės
ECALTA netirtas pacientams, sergantiems endokarditu, osteomielitu ar meningitu nuo Candida.
ECALTA veiksmingumas buvo įvertintas tik nedaugeliui neutropenija sergančių pacientų (žr. 5.1 skyrių).
Poveikis kepenims
Sveikiems asmenims ir pacientams, gydytiems anidulafunginu, pastebėtas kepenų fermentų koncentracijos padidėjimas. Kliniškai reikšmingi kepenų pakitimai pasireiškė kai kuriems pacientams, sergantiems sunkiomis ligomis, gydomiems keliais kartu vartojamais vaistiniais preparatais kartu su anidulafunginu. Klinikinių tyrimų metu retai pasireiškė reikšmingos kepenų funkcijos sutrikimo, hepatito ir kepenų nepakankamumo epizodai. Pacientai, kuriems gydymo anidulafunginu metu yra padidėjęs kepenų fermentų aktyvumas, turi būti stebimi dėl galimo kepenų funkcijos pablogėjimo ir įvertinamas tolesnio gydymo anidulafunginu rizikos ir naudos santykis.
Anafilaksinės reakcijos
Vartojant anidulafungino, buvo pranešta apie anafilaksines reakcijas, įskaitant šoką. Jei tokios reakcijos atsiranda, anidulafungino vartojimą reikia nutraukti ir taikyti tinkamą gydymą.
Su infuzija susijusios reakcijos
Gydymo anidulafunginu metu buvo pranešta apie su infuzija susijusias nepageidaujamas reakcijas, įskaitant bėrimą, dilgėlinę, paraudimą, niežėjimą, dusulį, bronchų spazmą ir hipotenziją. Su infuzija susijusios nepageidaujamos reakcijos yra retos, kai infuzijos greitis neviršija 1, 1 mg / min.
Su ikiklinikiniais tyrimais (žiurkėms) pastebėtas su infuzija susijusių reakcijų pablogėjimas (žr. 5.3 skyrių). Klinikinė šio poveikio reikšmė nežinoma. Tačiau reikia būti atsargiems, kai anidulafungino vartojama kartu su anestetikai.
Fruktozės turinys
Pacientai, turintys retą paveldimą fruktozės netoleravimą, neturėtų vartoti šio vaisto.
04.5 Sąveika su kitais vaistiniais preparatais ir kitos sąveikos formos
Anidulafunginas nėra kliniškai svarbus citochromo P450 izofermentų (1A2, 2B6, 2C8, 2C9, 2C19, 2D6, 3A) substratas, induktorius ar inhibitorius. Svarbu pažymėti, kad studijos į in vitro jie visiškai neatmeta sąveikos galimybės in vivo.
Buvo atlikti sąveikos tyrimai su anidulafunginu ir kitais vaistiniais preparatais, kuriuos galima vartoti kartu. Šių vaistinių preparatų ar anidulafungino dozės nerekomenduojama vartoti kartu su ciklosporinu, vorikonazolu ir takrolimuzu, o anidulafungino dozės nerekomenduojama vartoti kartu su amfotericinu B ar rifampicinu.
Vaikų populiacija
Sąveikos tyrimai buvo atlikti tik suaugusiems.
04.6 Nėštumas ir žindymo laikotarpis
Nėštumas
Nėra pakankamai duomenų apie anidulafungino vartojimą nėščioms moterims.
Triušiams, nėštumo metu gydytiems andidulafunginu, pastebėtas silpnas vystymosi poveikis, kai buvo toksiška patelėms (žr. 5.3 skyrių). Galima rizika žmonėms nežinoma. Todėl anidulafungino vartoti nėštumo metu nerekomenduojama.
Maitinimo laikas
Tyrimai su gyvūnais parodė, kad anidulafungino patenka į motinos pieną. Nežinoma, ar anidulafungino patenka į motinos pieną. Sprendimą tęsti / nutraukti žindymą ar gydymą anidulafunginu reikia priimti atsižvelgiant į žindymo naudą vaikui ir gydymo anidulafunginu naudą motinai.
Vaisingumas
Tyrimų su žiurkių patinais ir patelėmis metu anidulafungino poveikio vaisingumui nepastebėta (žr. 5.3 skyrių).
04.7 Poveikis gebėjimui vairuoti ir valdyti mechanizmus
Gebėjimo vairuoti ir valdyti mechanizmus tyrimų neatlikta.
04.8 Nepageidaujamas poveikis
Saugos profilio santrauka
Klinikinių tyrimų metu penkiolika šimtų šešiasdešimt penki tiriamieji buvo gydomi vienkartine ar daugkartine intraveninio anidulafungino doze: 1308 pacientai 2/3 fazės klinikiniuose tyrimuose (923 pacientai, sergantys invazine kandidozė / kandidozė, 355 pacientai, sergantys burnos / stemplės kandidoze, 30 pacientų invazinė aspergiliozė) ir 257 pacientai 1 fazės tyrimuose.
9 tyrimų metu anidulafungino saugumo profilis pagrįstas 840 pacientų, sergančių invazine kandidemija / kandidoze, gydoma rekomenduojama 100 mg paros doze. Iš pradžių 3 tyrimuose (vienas lyginamasis prieš flukonazolas, du nelyginamieji) buvo ištirti 204 pacientai; vidutinė gydymo į veną trukmė šiems pacientams buvo 13,5 dienos (nuo 1 iki 38 dienų), o 119 pacientų buvo gydomi anidulafunginu ≥ 14 dienų. Kituose 6 tyrimuose (du lyginamieji prieš kaspofungino ir keturi nepalyginamieji), buvo ištirti 636 pacientai, iš jų 53 neutropeniniai ir 131-giliųjų audinių infekcija; šiuose tyrimuose neutropenija sergantiems pacientams ir pacientams, sergantiems giliųjų audinių infekcija, vidutinė gydymo į veną trukmė buvo atitinkamai 10,0 (nuo 1 iki 42 intervalas) ir 14,0 (nuo 1 iki 42 intervalas). Nepageidaujamos reakcijos paprastai buvo lengvos ar vidutinio sunkumo ir retai nutraukdavo gydymą.
Klinikinių tyrimų metu, gydant anidulafunginu, buvo pranešta apie su infuzija susijusias nepageidaujamas reakcijas, kaip apibendrinta 1 lentelėje.
Nepageidaujamos reakcijos lentelėje
Žemiau esančioje lentelėje pateikiamos visų priežasčių nepageidaujamos reakcijos (MedDRA terminai), pastebėtos 840 tiriamųjų, gydytų 100 mg anidulafungino, atitinkamu dažniu labai dažni (≥ 1/10), dažni (nuo ≥ 1/100 iki
1 lentelė. Nepageidaujamų reakcijų lentelė
* Žr. 4.4 skyrių.
Pranešimas apie įtariamas nepageidaujamas reakcijas
Svarbu pranešti apie įtariamas nepageidaujamas reakcijas, atsiradusias po vaistinio preparato registravimo, nes tai leidžia nuolat stebėti vaisto naudos ir rizikos santykį. Sveikatos priežiūros specialistų prašoma pranešti apie bet kokias įtariamas nepageidaujamas reakcijas per nacionalinę pranešimo sistemą. .
04.9 Perdozavimas
Kaip ir bet kokio perdozavimo atveju, reikia imtis būtinų bendrųjų palaikomųjų priemonių.
Perdozavus, gali pasireikšti 4.8 skyriuje išvardytos nepageidaujamos reakcijos.
Klinikinių tyrimų metu vienkartinė 400 mg anidulafungino dozė buvo netyčia sušvirkšta kaip prisotinamoji dozė. Nepageidaujamų reakcijų nepastebėta. Tyrime, kuriame dalyvavo 10 sveikų savanorių, nepastebėta dozę ribojančio toksiškumo. Skyrė 260 mg įsotinamąją dozę, po to-130 mg per parą; 3 iš 10 tiriamųjų pranešė apie laikiną ir besimptomį transaminazių kiekio padidėjimą (≤ 3 x viršutinę normos ribą (VNR)).
ECALTA negalima dializuoti.
05.0 FARMAKOLOGINĖS SAVYBĖS
05.1 Farmakodinaminės savybės
Farmakoterapinė grupė: priešgrybeliniai vaistai sisteminiam vartojimui, kiti priešgrybeliniai vaistai sisteminiam vartojimui.
ATC kodas: JO2AX06.
Veiksmo mechanizmas
Anidulafunginas yra „pusiau sintetinis echinokandinas, lipopeptidas, susintetintas iš fermentacijos produkto“.Aspergillus nidulans.
Anidulafunginas selektyviai slopina beta-D-gliukano sintazę-fermentą, randamą grybelinėse, bet ne žinduolių ląstelėse. Tai apima "beta-D-gliukano, kuris yra esminė grybelinės ląstelės sienelės sudedamoji dalis, susidarymo slopinimą. Anidulafunginas parodė" fungicidinį poveikį Candida spp. ir „aktyvumas prieš aktyvias hifų ląstelių augimo sritis Aspergillus fumigatus.
Veikla in vitro
Anidulafunginas parodė „aktyvumą“ in vitro link C. albicans, C. glabrata, C. parapsilosis, C. krusei Ir C. tropicalis. Šių duomenų klinikinę reikšmę rasite skyriuje „Klinikinis veiksmingumas ir saugumas“ Aspergillus fumigatus.
Izolatai, turintys mutacijų tikslinio geno karštųjų taškų regionuose, buvo siejami su klinikinėmis nesėkmėmis ar naujai prasidėjusia grybeline infekcija (proveržis). Gydymas kaspofunginu yra susijęs su daugeliu klinikinių atvejų. Tačiau atliekant bandymus su gyvūnais šios mutacijos suteikia kryžminį atsparumą visiems trims echinokandinams, todėl kol nebus įgyta tolesnė klinikinė anidulafungino patirtis, šie izoliatai klasifikuojami kaip atsparūs echinokandinams.
Veikla in vitro anidulafungino prieš Candida jis nėra vienodas. Tiksliau, už C. parapsilozė Anidulafungino MIK (minimali slopinanti koncentracija) yra didesnė nei kitų rūšių Candida. „Europos jautrumo antimikrobinėms medžiagoms tyrimo komitetas (EUCAST) nustatė standartizuotą anidulafungino jautrumo rūšims tyrimo metodą Candida taip pat atitinkamus aiškinimo taškus.
2 lentelė. EUCAST ribinės vertės
1 C. parapsilozė turi „būdingą tikslinio geno pakitimą, kuris yra tikėtinas mechanizmas, atsakingas už didesnį MIK nei kitų rūšių Candida. Klinikinių tyrimų metu anidulafungino ir C. parapsilozė tačiau echinokandinų vartojimas sergant kandidemija statistiškai nesiskyrė nuo kitų rūšių C. parapsilozė tai gali būti nelaikoma pirmo pasirinkimo terapija
2 EUCAST nenustatė su rūšimi nesusijusių anidulafungino ribinių verčių
Veikla in vivo
Parenteraliai vartojamas anidulafunginas buvo veiksmingas prieš Candida Imunokompetentingų ir susilpnėjusių imunitetų pelių ir triušių modeliuose. Gydymas anidulafunginu pailgino išgyvenamumą ir sumažino naštą Candida spp. atitinkamame organe, kai nustatoma kas 24–96 valandas nuo paskutinio gydymo.
Laboratorinių gyvūnų tirtos infekcijos apėmė išplitusią infekciją C. albicans triušiams, sergantiems neutropenija, stemplės / burnos ir ryklės infekcijai triušiams su neutropenija C. albicans atsparios flukonazolui ir išplitusioms infekcijoms neutropeninėms pelėms C. glabrata atsparus flukonazolui.
Klinikinis veiksmingumas ir saugumas
Kandidemija ir kitos invazinės kandidozės formos
Anidulafungino saugumas ir veiksmingumas buvo įvertintas pagrindiniame, atsitiktinių imčių, dvigubai aklu, daugiacentriu, 3 fazės klinikiniu tyrimu, atliktu daugelyje šalių, daugiausia ne neutropenija sergantiems pacientams, sergantiems kandidemija, ir nedaugeliui pacientų, sergančių giliai įsišaknijusiomis infekcijomis. Candida lokalizuotas audiniuose arba susijęs su abscesų susidarymu. Pacientams, sergantiems endokarditu, osteomielitu ar meningitu nuo Candidaarba tiems, kurie serga infekcijomis nuo C. krusei, buvo išskirti iš tyrimo. Pacientai buvo atsitiktinai parinkti, kad gautų anidulafungino (200 mg įsotinamoji intraveninė dozė, po to 100 mg per parą į veną) arba flukonazolo (800 mg įsotinamoji dozė į veną, po to 400 mg per parą), ir buvo suskirstyti pagal APACHE II skalę (≤ 20 ir> 20). ir remiantis neutropenijos buvimu ar nebuvimu. Gydymas buvo atliekamas mažiausiai 14 dienų ir ne ilgiau kaip 42 dienas. Abiejų grupių pacientams buvo leista pereiti prie geriamojo flukonazolo po mažiausiai 10 dienų gydymo į veną, su sąlyga, kad jie toleravo geriamąjį gydymą ir mažiausiai 24 valandas buvo karščiavę, o naujausios kraujo kultūros buvo neigiamos. Candida spp.
Pacientai, kurie gavo bent vieną tiriamojo vaisto dozę ir kurių kultūra buvo teigiama Candida spp. iš įprastai sterilios vietos prieš įtraukiant į tyrimą buvo įtraukti į modifikuoto gydymo tikslo (MITT) populiaciją. Pirminės veiksmingumo analizės metu (bendras atsakas gydymo į veną pabaigoje MITT populiacijose) anidulafunginas buvo lyginamas su flukonazolu apibrėžtas dviejų pakopų statistinis palyginimas (ne prastesnis, o po to-pranašumas). Sėkmingam bendram atsakui reikėjo klinikinio pagerėjimo ir mikrobiologinio išnaikinimo. Pacientai buvo stebimi šešias savaites po viso gydymo pabaigos.
Du šimtai penkiasdešimt šeši pacientai, kurių amžius nuo 16 iki 91 metų, buvo atsitiktinai parinkti gydymui ir gavo bent vieną tiriamojo vaisto dozę. Pradinio vizito metu dažniausiai buvo izoliuotos rūšys C. albicans (63,8% anidulafungino, 59,3% flukonazolo), po to C. glabrata (15,7 %, 25,4 %), C. parapsilozė (10,2%, 13,6%) e C. tropicalis (11,8%, 9,3%) - atitinkamai 20, 13 ir 15 paskutinių 3 anidulafungino grupės rūšių. Daugumos pacientų APACHE II balas buvo ≤ 20, o labai nedaug pacientų buvo neutropeniniai.
Veiksmingumo duomenys, tiek bendri, tiek susiję su įvairiais pogrupiais, pateikti žemiau 3 lentelėje.
a Apskaičiuota kaip anidulafunginas, atėmus flukonazolą
b Kartu su kandidoze ar be jos
c Pilvo viduje
d Duomenys apie pacientus, kurių pradžioje buvo vienas patogenas
ir 98,3% pasikliautinųjų intervalų, kai vėliau buvo atlikti keli palyginimai atliekant post-hoc analizę.
Mirtingumas tiek anidulafungino, tiek flukonazolo grupėse parodytas 4 lentelėje:
Papildomi duomenys apie pacientus, sergančius neutropenija
Anidulafungino (200 mg įsotinamoji dozė į veną, po to 100 mg per parą į veną) veiksmingumas suaugusiems pacientams, sergantiems neutropenija (kai absoliutus neutrofilų skaičius yra ≤ 500 ląstelių / mm3, baltųjų kraujo kūnelių ≤ 500 ląstelių / mm3 arba tyrėjas, pradiniame etape priskiriamas neutropenijai). mikrobiologiškai patvirtinta invazinė kandidozė buvo įvertinta atliekant 5 bendrų 5 perspektyvinių tyrimų analizę (1 lyginamoji prieš kaspofungino ir 4 atviros, nelyginamosios). Pacientai buvo gydomi mažiausiai 14 dienų. Kliniškai stabiliems pacientams buvo galima pereiti prie geriamojo azolo terapijos praėjus mažiausiai 5-10 dienų po gydymo anidulafunginu. Iš viso į analizę buvo įtraukti 46 pacientai. Dauguma pacientų turėjo tik kandidemiją (84,8%; 39/46). Pradžioje dažniausiai išskirti patogenai buvo C. tropicalis (34,8%; 16/46), C. krusei (19,6%; 9/46), C. parapsilozė (17,4%; 8/46), C. albicans (15,2%; 7/46) ir C. glabrata (15,2%; 7/46). Bendras sėkmingo atsako dažnis gydymo į veną pabaigoje (pirminė vertinamoji baigtis) buvo 26/46 (56,5%), o visų gydymo pabaigoje - 24/46 (52,2%). Visų priežasčių mirtingumas iki tyrimo pabaigos (6 savaičių stebėjimo vizitas) buvo 21/46 (45,7%).
Anidulafungino veiksmingumas suaugusiems pacientams, sergantiems neutropenija (nustatytas absoliutus neutrofilų skaičius ≤ 500 ląstelių / mm3 pradžioje), kuriems buvo invazinė kandidozė, buvo įvertintas perspektyviame, kontroliuojamame, dvigubai aklo, atsitiktinių imčių tyrime.Tinkami pacientai buvo gydomi anidulafunginu (200 mg įsotinamoji intraveninė dozė, po to 100 mg per parą į veną) arba kaspofunginu (70 mg įsotinamoji intraveninė dozė, po to 50 mg per parą į veną) (atsitiktinė atranka 2: 1). Pacientai buvo gydomi mažiausiai 14 dienų.
Kliniškai stabiliems pacientams buvo leista pereiti prie geriamojo azolo terapijos praėjus mažiausiai 10 gydymo dienų. Iš viso tyrime dalyvavo 14 pacientų, sergančių neutropenija, kuriems buvo mikrobiologiškai patvirtinta invazinė kandidozė (MITT populiacija) (11 anidulafungino, kaspofungino). Dauguma pacientų sirgo vien kandidoze. Ligos sukėlėjai dažniausiai buvo išskirti iš pradžių C. tropicalis (4 anidulafungino, 0 kaspofungino), C.. parapsilozė (2 anidulafunginas, 1 kaspofunginas), C. krusei (2 anidulafunginas, 1 kaspofunginas) C. ciferrii (2 anidulafungino, 0 kaspofungino). Bendras sėkmingo atsako dažnis gydymo į veną pabaigoje (pirminė baigtis) buvo 8/11 (72,7%) anidulafungino ir 3/3 (100%) kaspofungino (skirtumas -27,3, 95%PI: -80,9, 40,3); bendras gydymo sėkmės rodiklis visų gydymo pabaigoje buvo 8/11 (72,7%) anidulafungino ir 3/100%) kaspofungino (skirtumas -27,3, 95%PI: -80, 9, 40,3). Visų priežasčių mirtingumas iki 6 savaičių stebėjimo anidulafungino (MITT populiacija) buvo 4/11 (36,4%) ir 2/3 (66,7%)-kaspofungino.
Pacientai, turintys mikrobiologiškai patvirtintą invazinę kandidozę (MITT populiaciją) ir neutropeniją, buvo nustatyti atliekant 4 panašiai suplanuotų, atvirų, nelyginamųjų perspektyvinių tyrimų bendrą analizę. Anidulafungino veiksmingumas (200 mg įsotinamoji dozė į veną, po to 100 mg dieną į veną) buvo vertinamas 35 apibrėžtiems suaugusiems neutropenija sergantiems pacientams, kurių absoliutus neutrofilų skaičius buvo ≤ 500 ląstelių / mm3, arba 22 pacientams, kurių leukocitų skaičius buvo ≤ 500 ląstelių / mm3, arba 13 tyrėjų klasifikuotų pacientų, kuriems tyrimo pradžioje buvo neutropenija. Pacientai buvo gydomi mažiausiai 14 dienų. Kliniškai stabiliems pacientams buvo galima pereiti prie geriamojo azolo terapijos praėjus mažiausiai 5-10 dienų po gydymo anidulafunginu. Dauguma pacientų sirgo vien kandidoze (85,7%). Ligos sukėlėjai dažniausiai buvo išskirti iš pradžių C. tropicalis (12 pacientų), C. albicans (7 pacientai), C. glabrata (7 pacientai), C. krusei (7 pacientai) e C. parapsilozė (6 pacientai). Bendras sėkmingo atsako dažnis gydymo į veną pabaigoje (pirminė vertinamoji baigtis) buvo 18/35 (51,4%) ir 16/35 (45,7%) visų gydymo pabaigoje. Visų priežasčių mirtingumas 28 dieną buvo 10/35 (28,6%). Bendras sėkmingo atsako dažnis gydymo į veną pabaigoje ir visų gydymo kursų pabaigoje buvo 7/13 (53,8%) abiems iš 13 pacientų, kuriuos tyrėjas pradžioje klasifikavo kaip neutropeninius.
Papildomi duomenys apie pacientus, sergančius giliųjų audinių infekcijomis
Anidulafungino (200 mg įsotinamoji dozė į veną, po to 100 mg per parą į veną) veiksmingumas suaugusiems pacientams, sergantiems mikrobiologiškai patvirtinta giliųjų audinių kandidoze, buvo įvertintas atlikus 5 panašių planų (1 lyginamasis ir 4 atviras) tyrimus. Pacientai buvo gydomi mažiausiai 14 dienų. Atliekant 4 atvirus tyrimus, perėjimas prie geriamojo azolo buvo leidžiamas praėjus mažiausiai 5-10 dienų po gydymo anidulafunginu. Iš viso į analizę buvo įtraukti 129 pacientai. Dvidešimt vienas pacientas (16,3%) kartu sirgo kandidemija. Vidutinis APACHE II balas buvo 14,9 (2-44 intervalas). Dažniausios infekcijos vietos buvo pilvaplėvės ertmė 54,3%, 70/129), kepenų ir tulžies takus (7,0%, 9/129), pleuros ertmę (5,4%, 7/129) ir inkstus (3,1%, 4/129). Ligos sukėlėjai, dažniausiai nustatyti iš giliųjų audinių, buvo C. albicans (64,3%; 83/129), C. glabrata (31,0%; 40/129), C. tropicalis (11,6%; 15/129) e C. krusei (5,4%; 7/129). 5 lentelėje pateikiamas bendras sėkmės rodiklis gydymo į veną pabaigoje (pirminė vertinamoji baigtis) ir visų gydymo pabaigoje, taip pat mirtingumas nuo visų priežasčių iki 6 savaičių stebėjimo vizito.
a Bendras sėkmės atsakas buvo apibrėžiamas kaip klinikinė ir mikrobiologinė sėkmė
b EOIVT, gydymo į veną pabaiga; EOT, viso gydymo pabaiga
05.2 Farmakokinetinės savybės
Bendrosios farmakokinetikos savybės
Anidulafungino farmakokinetika būdinga sveikiems savanoriams, ypatingoms populiacijoms ir pacientams. Sisteminės ekspozicijos metu buvo pastebėtas mažas kintamumas tarp asmenų (variacijos koeficientas? 25%) pastovi būsena buvo pasiekta pirmą dieną po įsotinamosios dozės (dvigubai didesnės už palaikomąją dozę).
Paskirstymas
Anidulafungino farmakokinetikai būdingas greitas pasiskirstymo pusinės eliminacijos laikas (0,5–1 val.) Ir pasiskirstymo tūris 30–50 l, kuris yra panašus į viso organizmo skysčio tūrį.
Anidulafunginas plačiai (> 99%) jungiasi su plazmos baltymais. Specifinių anidulafungino pasiskirstymo audiniuose žmonių tyrimų neatlikta, todėl nėra informacijos apie anidulafungino įsiskverbimą į smegenų skystį ir (arba) per kraujo ir smegenų barjerą.
Biotransformacija
Anidulafungino metabolizmo kepenyse nepastebėta. Anidulafunginas nėra kliniškai svarbus citochromo P450 izofermentų substratas, induktorius ar inhibitorius. Mažai tikėtina, kad anidulafunginas turėtų kliniškai reikšmingą poveikį vaistų, kuriuos metabolizuoja citochromo P450 izofermentai, metabolizmui.
Anidulafunginas lėtai chemiškai skaidantis fiziologinėje temperatūroje ir pH paverčiamas atviro ciklo peptidu, neturinčiu priešgrybelinio aktyvumo. Skilimo pusinės eliminacijos laikas in vitro fiziologinėmis sąlygomis anidulafungino yra apie 24 val. Atviros kilpos produktas in vivovėliau jis paverčiamas peptidus ardančiomis medžiagomis ir pašalinamas daugiausia išsiskyrus su tulžimi.
Eliminavimas
Anidulafungino klirensas yra maždaug 1 l / val. Anidulafungino pusinės eliminacijos laikas yra maždaug 24 valandos, kuri apibūdina didžiąją dalį koncentracijos plazmoje ir 40-50 valandų galutinis pusinės eliminacijos periodas, apibūdinantis galutinę profilio eliminacijos fazę.
Vienos dozės klinikinio tyrimo metu sveikiems savanoriams buvo skiriamas radioaktyviai pažymėtas (14C) anidulafunginas (≥ 88 mg). Maždaug 30% suleistos radioaktyviosios dozės per 9 dienas buvo pašalinta su išmatomis, o mažiau kaip 10% dozės išsiskyrė nepakitusio vaisto pavidalu. Mažiau nei 1% pavartotos radioaktyviosios dozės išsiskyrė su šlapimu, o tai rodo, kad inkstų klirensas yra nereikšmingas. . Praėjus 6 dienoms po vartojimo, anidulafungino koncentracija nukrito žemiau apatinių kiekybinio nustatymo ribų. Praėjus 8 savaitėms po vartojimo kraujyje, šlapime ir išmatose buvo pastebėtas nedidelis kiekis iš vaistinio preparato gauto radioaktyvumo.
Tiesiškumas
Anidulafungino farmakokinetika įvairiose vienkartinėse paros dozėse (15-130 mg) yra tiesinė.
Specialios pacientų grupės
Pacientams, sergantiems grybelinėmis infekcijomis
Pacientų, sergančių grybelinėmis infekcijomis, anidulafungino farmakokinetika yra panaši į tą, kuri nustatyta sveikų asmenų, remiantis populiacijos farmakokinetikos analize. Vartojant 200/100 mg paros dozavimo schemą, kai infuzijos greitis yra 1,1 mg / min., Cmax - pastovi būsena ir mažiausia koncentracija (Cmin) pasiekė atitinkamai 7 ir 3 mg / l, o vidutinis AUC buvo pastovi būsena apie 110 mg • h / l.
Svoris
Nors populiacijos farmakokinetikos analizė parodė, kad svoris yra klirenso kintamumo šaltinis, anidulafungino farmakokinetikai svoris turi minimalią klinikinę reikšmę.
Priklausymo lytis
Savanorių vyrų ir moterų anidulafungino koncentracija plazmoje buvo panaši. Atliekant tyrimus, kuriuose dalyvavo kelių dozių pacientai, vyrų klirensas buvo šiek tiek greitesnis (maždaug 22%).
Vyresnio amžiaus piliečiai
Populiacijos farmakokinetikos analizė parodė, kad vidutinis klirensas šiek tiek skyrėsi tarp senyvo amžiaus žmonių (amžius ≥ 65 metų, vidutinė CL = 1,07 l / h) ir ne pagyvenusių žmonių (amžius
Lenktynės
Anidulafungino farmakokinetika buvo panaši tarp baltųjų, juodųjų, azijiečių ir ispanų.
ŽIV pozityvumas
ŽIV užsikrėtusiems pacientams dozės koreguoti nereikia, nepaisant kartu vartojamo antiretrovirusinio gydymo.
Kepenų nepakankamumas
Kepenys anidulafungino nemetabolizuoja. Anidulafungino farmakokinetika buvo tiriama tiriant asmenis, kuriems buvo A, B ar C laipsnio Child-Pugh laipsnio kepenų funkcijos sutrikimas.
Nors pacientams, sergantiems C laipsnio Child-Pugh kepenų funkcijos sutrikimu, buvo pastebėtas nedidelis AUC sumažėjimas, sumažėjimas atitiko sveikų asmenų populiacijos įvertinimo ribas.
Inkstų nepakankamumas
Anidulafungino inkstų klirensas yra nereikšmingas (normali inkstų funkcija. Anidulafungino negalima dializuoti ir jį galima skirti nepriklausomai nuo to, kada atliekama dializė.
Vaikams
Anidulafungino farmakokinetika, išgėrus mažiausiai 5 paros dozes, buvo tiriama 24 vaikams, kurių imuninė sistema sutrikusi (2-11 metų amžiaus) ir paaugliams (12-17 metų), sergantiems neutropenija. The pastovus buvo pasiekta pirmą dieną po įsotinamosios dozės (dvigubai didesnės už palaikomąją dozę) ir Cmax bei AUCss pastovi būsena padidėjo proporcingai dozei. Sisteminė ekspozicija, suvartojus 0,75 mg ir 1,5 mg / kg per parą palaikomąją dozę šioje populiacijoje, buvo panaši į tą, kuri buvo pastebėta suaugusiems žmonėms, atitinkamai vartojant 50 ir 100 mg per parą. Šie pacientai gerai toleravo abi dozavimo schemas.
05.3 Ikiklinikinių saugumo duomenys
3 mėnesių trukmės tyrimų metu žiurkėms ir beždžionėms, gydytoms dozėmis, kurios buvo 4–6 kartus didesnės už numatomą klinikinę terapinę ekspoziciją, buvo pastebėtas toksinis poveikis kepenims, įskaitant fermentų padidėjimą ir morfologinius pokyčius. in vitro Ir in vivo su anidulafunginu nepateikė jokių genotoksinio poveikio įrodymų. Ilgalaikiai tyrimai su gyvūnais nebuvo atlikti siekiant įvertinti kancerogeninį anidulafungino potencialą.
Anidulafungino skyrimas žiurkėms neparodė jokio poveikio reprodukcijai, įskaitant patinų ir patelių vaisingumą.
Anidulafunginas peržengė placentos barjerą žiurkėms ir buvo aptiktas vaisiaus plazmoje.
Embriono ir vaisiaus vystymosi tyrimai buvo atlikti naudojant dozes nuo 0,2 iki 2 kartų (žiurkėms) ir nuo 1 iki 4 kartų (triušiams) siūlomą palaikomąją 100 mg paros dozę. Anidulafunginas nesukėlė jokio su vaistais susijusio toksiškumo vystymuisi žiurkėms, tirtoms naudojant didžiausią dozę. Triušiams pastebėtas vystymosi poveikis (šiek tiek sumažėjęs kūno svoris) pasireiškė tik vartojant didžiausią tirtą dozę, kuri taip pat sukėlė toksiškumą motinai.
Neinfekuotoms suaugusioms ir naujagimių žiurkėms po vienkartinės dozės smegenų anidulafungino koncentracija buvo maža (smegenų ir plazmos santykis maždaug 0,2). Tačiau neinfekuotų naujagimių žiurkių smegenų koncentracija padidėjo po 5 paros dozių (smegenų ir plazmos santykis maždaug 0,7). Kelių dozių tyrimų metu triušiai, sergantys išplitusi kandidoze, ir pelės, sergančios CNS infekcija, kurią sukėlė Candida, anidulafunginas sumažino grybelio krūvį smegenyse.
Žiurkės buvo gydomos trimis anidulafungino dozėmis ir anestezuojamos per vieną valandą, naudojant ketamino ir ksilazino derinį. Didesnės dozės grupės žiurkės pranešė apie su infuzija susijusias reakcijas, kurias sustiprino anestezija. Kai kurios vidutinės dozės grupės žiurkės pranešė apie panašias reakcijas, tačiau tik po anestezijos.
Nepageidaujamų reakcijų nebuvo pranešta gyvūnams, gydytiems mažesne doze, esant anestezijai ar be jos, o vidutinės dozės grupėje, jei nebuvo anestezijos, su infuzija susijusių reakcijų nepasireiškė.
06.0 FARMACINĖ INFORMACIJA
06.1 Pagalbinės medžiagos
Fruktozė
Manitolis
Polisorbatas 80
Vyno rūgštis
Natrio hidroksidas (pH koreguoti)
Vandenilio chlorido rūgštis (pH koreguoti)
06.2 Nesuderinamumas
Šio vaistinio preparato negalima maišyti su kitais produktais, išskyrus išvardytus 6.6 skyriuje.
06.3 Galiojimo laikas
3 metai.
Leidžiama atlikti temperatūros pokyčius 96 valandas iki 25 ° C, o miltelius galima grąžinti į šaldymo sąlygas.
Paruoštas tirpalas:
Paruoštą tirpalą galima laikyti iki 25 ° C temperatūroje iki 24 valandų.
Paruoštas paruošto tirpalo cheminis ir fizinis stabilumas 25 ° C temperatūroje išlieka 24 valandas.
Mikrobiologiniu požiūriu, laikantis optimalių aseptinių sąlygų, paruoštą tirpalą galima naudoti iki 24 valandų, jei jis laikomas 25 ° C temperatūroje.
Infuzinis tirpalas:
Infuzinį tirpalą galima laikyti 48 valandas 25 ° C temperatūroje arba mažiausiai 72 valandas užšaldyti.
Naudojamo infuzinio tirpalo cheminis ir fizinis stabilumas buvo įrodytas 48 valandas esant 25 ° C temperatūrai.
Mikrobiologiniu požiūriu, laikantis optimalių aseptinių sąlygų, infuzinis tirpalas gali būti naudojamas 48 valandas po paruošimo, jei laikomas 25 ° C temperatūroje.
06.4 Specialios laikymo sąlygos
Laikyti šaldytuve (2 ° C - 8 ° C).
Paruošto ir praskiesto vaistinio preparato laikymo sąlygos pateiktos 6.3 skyriuje.
06.5 Pirminės pakuotės pobūdis ir pakuotės turinys
30 ml I tipo stiklo buteliukas su elastomeriniu kamščiu (butilo guma su inertiška polimero danga ant paviršiaus, liečiančio produktą, ir su tepalu viršutiniame paviršiuje, kad būtų lengviau gaminti) ir aliuminio sandarikliu su nuimamu dangteliu.
Pakuotėje 1 buteliukas.
06.6 Naudojimo ir naudojimo instrukcijos
Nėra specialių nurodymų, kaip jį sunaikinti.
ECALTA reikia ištirpinti injekciniu vandeniu ir po to praskiesti 9 mg / ml (0,9%) natrio chlorido injekciniu tirpalu TIK 50 mg / ml (5%) gliukozės infuzijai. Ištirpinto ECALTA suderinamumas su intraveninėmis medžiagomis, priedais ar vaistiniais preparatais, išskyrus 9 mg / ml (0,9%) natrio chlorido arba 50 mg / ml (5%) gliukozės, nenustatytas.
Paruošimas
Kiekvieną buteliuką reikia aseptinėmis sąlygomis ištirpinti 30 ml injekcinio vandens, kad būtų pasiekta 3,33 mg / ml koncentracija. Paruošimo laikas gali trukti iki 5 minučių. Po to praskiedimo tirpalą reikia išmesti, jei nustatomos dalelės ar spalvos pasikeitimas.
Skiedimas ir infuzija
Paruoštą buteliuką reikia aseptinėmis sąlygomis perkelti į intraveninį maišelį (arba buteliuką), kuriame yra 9 mg / ml (0,9%) infuzinio natrio chlorido arba 50 mg / ml 5%gliukozės), kad būtų pasiekta koncentracija. 0,77 mg / ml anidulafungino. Žemiau esančioje lentelėje parodytas kiekvienai dozei reikalingas tūris.
Skiedimo reikalavimai vartojant ECALTA
Natrio chloridas infuzijai 9 mg / ml (0,9%) arba gliukozė infuzijai 50 mg / ml (5%)
B Infuzinio tirpalo koncentracija yra 0,77 mg / ml
Infuzijos greitis neturi viršyti 1,1 mg / min. (Atitinka 1,4 ml / min., Ištirpinus ir praskiedus, kaip nurodyta) (žr. 4.2, 4.4 ir 4.8 skyrius).
Kai tik leidžia tirpalas ir talpykla, prieš vartojant parenteralinius vaistinius preparatus reikia vizualiai apžiūrėti, ar nėra dalelių ar spalvos pakitimų.
Nepanaudotą vaistą ir jo atliekas reikia sunaikinti laikantis vietinių taisyklių
07.0 RINKODAROS TEISĖS TURĖTOJAS
„Pfizer Limited“
Ramsgate Road, Sandwich
Kent, CT13 9NJ, Jungtinė Karalystė.
08.0 RINKODAROS TEISĖS NUMERIS
EU/1/07/416/002
038382026
09.0 RINKODAROS TEISĖS SUTEIKIMO AR PATVIRTINIMO DATA
Registravimo data: 2007 m. Rugsėjo 20 d
Paskutinio atnaujinimo data: 2012 m. Rugpjūčio 23 d
10.0 TEKSTO PERŽIŪROS DATA
2014 m. Rugpjūčio 26 d