Apibrėžimas
Fermentai yra baltymai, gaminami augalų ir gyvūnų ląstelėse, kurie veikia kaip katalizatoriai, pagreitindami biologines reakcijas, jų nekeičiant.
Fermentai veikia jungdamiesi su konkrečia medžiaga, kad ją paverstų kita medžiaga; klasikinius pavyzdžius pateikia virškinimo fermentai, esantys seilėse, skrandyje, kasoje ir plonojoje žarnoje, kurie atlieka esminę virškinimo funkciją ir padeda suskaidyti maistą į pagrindines sudedamąsias dalis, kurias vėliau organizmas gali įsisavinti ir panaudoti, apdoroti kitais fermentais arba išsiskiria kaip atliekos.
Kiekvienas fermentas atlieka specifinį vaidmenį: pavyzdžiui, tas, kuris skaido riebalus, neveikia baltymų ar angliavandenių. Fermentai yra būtini organizmo gerovei. Net vieno fermento trūkumas gali sukelti rimtų sutrikimų. Gerai žinomas pavyzdys yra fenilketonurija (PKU), liga, kuriai būdingas nesugebėjimas metabolizuoti nepakeičiamos amino rūgšties, fenilalaninas, kurio susikaupimas gali sukelti fizines deformacijas ir psichines ligas.
Biocheminis tyrimas
Fermentai yra tam tikri baltymai, kuriems būdingi biologiniai katalizatoriai, tai yra, jie turi galimybę suskaidyti reakcijos aktyvinimo energiją (Eatt), pakeisdami jos kelią taip, kad kinetiškai lėtas procesas vyktų greičiau.
Fermentai padidina termodinamiškai galimų reakcijų kinetiką ir, skirtingai nei katalizatoriai, yra daugiau ar mažiau specifiški: todėl jie turi substrato specifiškumą.
Fermentas nedalyvauja reakcijos stechiometrijoje: kad tai įvyktų, galutinė katalizinė vieta turi būti identiška pradinei.
Katalizinio veikimo metu beveik visada yra lėta fazė, kuri lemia proceso greitį.
Kai mes kalbame apie fermentus, nėra teisinga kalbėti apie pusiausvyros reakcijas, o vietoj to pastovi būsena (būsena, kai tam tikras metabolitas susidaro ir nuolat vartojamas, laikui bėgant išlaikant jo koncentraciją beveik pastovią). Reakcijos produktas, katalizuojamas vieno fermento, dažniausiai pats yra reagavimo medžiaga tolesnei reakcijai, katalizuojamas kito fermento ir pan.
Fermentų katalizuojami procesai paprastai susideda iš reakcijų sekų.
Bendrą reakciją, kurią katalizuoja fermentas (E), galima apibendrinti taip:

E yra fermentas
S yra substratas;
ES reiškia aduktą tarp fermento ir substrato;
P yra produktas;
K yra reakcijos greičio konstanta.
Bendrasis fermentas (E) susijungia su substratu (S), sudarydamas aduktą (ES) su greičio konstanta K1; jis gali vėl disocijuoti į E + S, esant greičio konstantai K2, arba (jei „gyvena“ pakankamai ilgai) ) gali pereiti prie P formos su greičio konstanta K3.
Produktas (P) savo ruožtu gali rekombinuotis su fermentu ir reformuoti adduktą greičio konstanta K4.
Sumaišius fermentą ir substratą, yra dalis laiko, kai abiejų rūšių susitikimas dar neįvyko: tai yra, labai trumpas laiko intervalas (kuris priklauso nuo reakcijos), kuriame fermentas ir substratas turi dar neįvykdytas; po šio laikotarpio fermentas ir substratas vis dažniau liečiasi ir susidaro ES adduktas. Vėliau fermentas veikia substratą ir produktas išsiskiria. Tada galima sakyti, kad c "yra pradinis laiko intervalas, per kurį ES addukto koncentracija negali būti apibrėžta; po šio laikotarpio daroma prielaida, kad pastovi būsena yra nustatytas, tai yra, procesų, dėl kurių gaunamas adduktas, greitis yra lygus procesų, dėl kurių adduktas sunaikinamas, greičiui.
Michaelio-Menteno konstanta (KM) yra pusiausvyros konstanta (nurodyta pirmoje aukščiau aprašytoje pusiausvyroje); gerai apytiksliai galima pasakyti (nes taip pat reikėtų atsižvelgti į K3), kad KM pavaizduotas santykis tarp kinetinių konstantų K2 ir K1 (nurodo addukto ES sunaikinimą ir susidarymą pirmoje aukščiau aprašytoje pusiausvyroje) .
Per Michaelio-Menteno konstantą mes „nurodome afinitetą tarp fermento ir substrato: jei KM yra mažas c“ yra „didelis afinitetas tarp fermento ir substrato, tada ES adduktas yra stabilus.
Fermentai yra reguliuojami (arba moduliuojami).
Anksčiau daugiausia buvo kalbama apie neigiamą moduliaciją, tai yra, fermento katalizinių gebėjimų slopinimą, tačiau gali būti ir teigiamas moduliavimas, tai yra, yra rūšių, galinčių sustiprinti katalizines fermento galimybes.
Yra 4 slopinimo tipai (gauti iš modelio aproksimacijų, kad eksperimentiniai duomenys atitiktų matematines lygtis):
- konkurencinis slopinimas
- nekonkurencinis slopinimas
- nekonkurencingas slopinimas
- konkurencijos slopinimas
Mes kalbame apie konkurencinį slopinimą, kai molekulė (inhibitorius) gali konkuruoti su substratu. Dėl struktūrinio panašumo inhibitorius gali reaguoti vietoj substrato, taigi ir terminas „konkurencinis slopinimas“. Tikimybė, kad fermentas prisijungs prie inhibitoriaus ar substrato, priklauso nuo abiejų koncentracijos ir jų afiniteto fermentui; todėl reakcijos greitis priklauso nuo šių veiksnių.
Norint gauti tokį patį reakcijos greitį kaip ir be inhibitoriaus, būtina turėti didesnę substrato koncentraciją.
Eksperimentiškai įrodyta, kad esant inhibitoriui Michaelio-Menteno konstanta padidėja.
Vietoj to, „nekonkurencinis slopinimas, sąveika tarp molekulės, kuri turėtų veikti kaip moduliatorius (teigiamas arba neigiamas inhibitorius), ir„ fermento, vyksta kitoje vietoje nei ta, kurioje vyksta sąveika tarp fermento ir substrato; todėl mes kalbame apie alosterinę moduliaciją (iš graikų kalbos allosteros → kita svetainė).
Jei inhibitorius prisijungia prie fermento, jis gali pakeisti fermento struktūrą ir atitinkamai sumažinti substrato prisijungimo prie fermento efektyvumą.
Šio tipo procese Michaelio-Menteno konstanta išlieka pastovi, nes ši vertė priklauso nuo fermento ir substrato pusiausvyros, ir net esant inhibitoriui, šios pusiausvyros nesikeičia.
Nekompetentingo slopinimo reiškinys yra retas; tipiškas nekompetentingas inhibitorius yra medžiaga, kuri grįžtamai jungiasi prie ES addukto ir sukelia ESI:

Substrato pertekliaus slopinimas kartais gali būti nekonkurencingas, nes taip atsitinka, kai antroji substrato molekulė prisijungia prie ES komplekso ir susidaro ESS kompleksas.
Kita vertus, konkurencingas inhibitorius gali prisijungti tik prie substrato fermento addukto, kaip ir ankstesniu atveju: substrato prisijungimas prie laisvo fermento sukelia konformacinę modifikaciją, dėl kurios vieta yra prieinama inhibitoriui.
Michaelio Menteno konstanta mažėja didėjant inhibitoriaus koncentracijai: todėl, matyt, didėja fermento afinitetas substratui.
Serino proteazė
Jie yra fermentų šeima, kuriai priklauso chimotripsinas ir tripsinas.
Chimotripsinas yra proteolitinis ir hidrolizinis fermentas, kuris į dešinę pjauna hidrofobines ir aromatines aminorūgštis.
Chimotripsiną koduojančio geno produktas nėra aktyvus (jis aktyvuojamas su komanda); neaktyvią chimotripsino formą sudaro 245 aminorūgščių polipeptidinė grandinė. Chimotripsinas yra rutulio formos dėl penkių disulfidinių tiltų ir kitų nedidelių sąveikų (elektrostatinių, Van der Waals jėgų, vandenilio jungčių ir kt.).
Chimotripsiną gamina kasos chimozės ląstelės, kuriose jis yra specialiose membranose ir per kasos kanalą į žarnyną pašalinamas maisto virškinimo metu: chimotripsinas iš tikrųjų yra virškinimo fermentas. Baltymai ir maistinės medžiagos, kuriuos mes gauname su maistu, yra virškinami, kad suskaidytų į mažesnes grandines ir būtų absorbuojami bei paverčiami energija (pvz., Amilazės ir proteazės suskaido maistines medžiagas į gliukozę ir aminorūgštis, kurios pasiekia ląsteles per kraujagysles) jie pasiekia vartų veną ir iš ten patenka į kepenis, kur toliau gydomi).
Fermentai gaminami neaktyvios formos ir aktyvuojami tik pasiekus „vietą, kurioje jie turi veikti“; pasibaigus veiksmui, jie išjungiami. Kai dezaktyvuotas fermentas negali būti iš naujo suaktyvintas: norint atlikti „tolesnį katalizinį poveikį, jis turi būti pakeistas“ kita fermento molekule.Jei chimitripsinas būtų gaminamas aktyvioje formoje jau kasoje, jis užpultų pastarąją: pankreatitas yra patologija, atsirandanti dėl virškinimo fermentų, kurie jau yra aktyvuoti kasoje (o ne reikiamose vietose); kai kurie iš jų, jei negydomi laiku, privesti prie mirties.
Chimotripsino ir visų serino proteazių katalizinis poveikis atsiranda dėl alkoholio anijono (-CH2O-) buvimo šoninėje serino grandinėje.
Serino proteazės šį pavadinimą gauna būtent todėl, kad jų katalizinį poveikį lemia serinas.
Kai visas fermentas atliks savo veikimą, prieš vėl pradėdamas veikti ant substrato, jis turi būti atkurtas vandeniu; serino „išsiskyrimas“ vandeniu yra lėčiausias proceso etapas, ir tai yra ši fazė kuris lemia katalizės greitį.
Katalizinis veiksmas vyksta dviem etapais:
- katijoninių savybių turinčio anijono (anijono alkoholato) susidarymas ir vėlesnis nukleofilinis ataka prieš karbonilo anglį (C = O), skaidant peptidinį ryšį ir susidarius esteriui;
- vandens ataka atkuriant katalizatorių (gali vėl atlikti savo katalizinį poveikį).
Įvairūs serino proteazių šeimai priklausantys fermentai gali būti sudaryti iš skirtingų aminorūgščių, tačiau visų jų katalizinę vietą žymi serino šoninės grandinės alkoholinis anijonas.
Serino proteazių pošeimį sudaro fermentai, dalyvaujantys krešėjime (kurį sudaro baltymų transformacija iš neaktyvios formos į „kitą aktyvią formą“). Šie fermentai užtikrina, kad krešėjimas būtų kuo efektyvesnis ir ribotas. erdvė ir laikas (krešėjimas turi įvykti greitai ir turi įvykti tik šalia pažeistos vietos). Koaguliacijoje dalyvaujantys fermentai aktyvuojami kaskadoje (nuo vieno fermento aktyvavimo gaunami milijardai fermentų: kiekvienas aktyvuotas fermentas , savo ruožtu aktyvuoja daugelį kitų fermentų).
Trombozė yra patologija, atsirandanti dėl sutrikusio krešėjimo fermentų veikimo: ją sukelia be reikalo (nes nėra sužalojimo) suaktyvėję krešėjimui naudojami fermentai.
Yra moduliuojantys (reguliuojantys) fermentai ir slopinantys fermentai kitiems fermentams: sąveikaudami su pastaraisiais, jie reguliuoja arba slopina jų veiklą; Net fermento produktas gali būti fermento inhibitorius. Taip pat yra fermentų, kurie veikia daugiau, tuo didesnis substratas.
Lizocimas
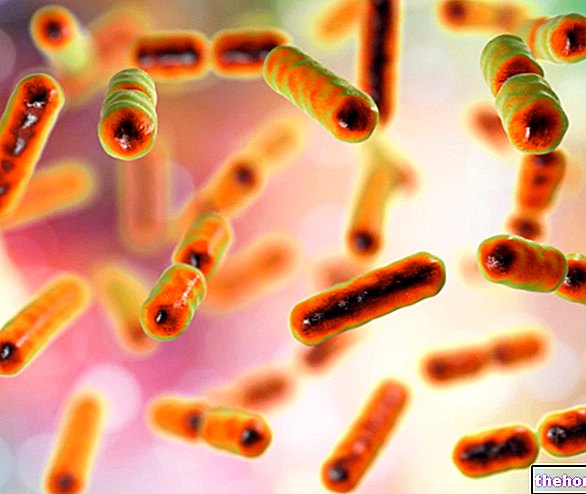
Luigi Pasteuras, čiaudėdamas ant Petri lėkštelės, atrado, kad gleivėse yra fermentų, galinčių naikinti bakterijas: lizocimas; iš graikų kalbos: liso = kokio dydžio; zimo = fermentas.
Lizocimas gali suskaidyti bakterijų ląstelių sieneles. Bakterijoms ir apskritai vienaląsčiams organizmams reikia mechaniškai atsparių struktūrų, kurios apribotų jų formą; bakterijų viduje yra labai didelis osmosinis slėgis, todėl jos pritraukia vandenį. Plazmos membrana sprogs, jei nebūtų ląstelės sienelės, kuri priešintųsi vandens patekimui ir apribotų bakterijos tūrį.
Ląstelės sienelę sudaro polisacharidinė grandinė, kurioje keičiasi N-acetil-gliukozamino (NAG) molekulės ir N-acetil-muramino rūgšties (NAM) molekulės; ryšys tarp NAG ir NAM nutrūksta hidrolizės būdu. NAM karboksilo grupė ląstelės sienelėje yra susijusi su peptidiniu ryšiu su aminorūgštimi.
Tarp įvairių grandinių susidaro tiltai, susidedantys iš pseudopeptidinių ryšių: išsišakojimas atsiranda dėl lizino molekulės; visa struktūra yra labai šakota ir tai suteikia jai didelį stabilumą.
Lizocimas yra antibiotikas (naikina bakterijas): jis veikia sukeldamas įtrūkimą bakterijų sienelėje; kai ši struktūra (kuri yra mechaniškai atspari) sulūžta, bakterija traukia vandenį, kol sprogsta. Lizocimas sugeba nutraukti β-1,4 gliukozidinį ryšį tarp NAM ir NAG.
Katalizinę lizocimo vietą vaizduoja griovelis, einantis išilgai fermento, į kurį įterpta polisacharidinė grandinė: į griovelį dedami šeši gliukozidiniai grandinės žiedai.
Trečioje griovelio padėtyje yra droselis: šioje padėtyje galima įdėti tik vieną NAG, nes aukštesnių matmenų NAM negali patekti. Tikroji katalizinė vieta yra tarp keturių ir penkių pozicijų: kadangi yra NAG trečioje padėtyje pjovimas įvyks tarp NAM ir NAG (o ne atvirkščiai); todėl pjūvis yra specifinis.
Optimalus lizocimo veikimo pH yra penki. Katalizinėje fermento vietoje, ty tarp keturių ir penkių pozicijų, yra asparto rūgšties ir glutamo rūgšties šoninės grandinės.
Homologijos laipsnis: matuoja baltymų struktūrų giminystę (t. Y. Panašumą).
Tarp lizocimo ir laktozės sintazės yra glaudus ryšys.
Laktozės sintetazė sintezuoja laktozę (kuri yra pagrindinis pieno cukrus): laktozė yra galaktozilo gliukozidas, kuriame c "yra β-1,4 gliukozidinis ryšys tarp galaktozės ir gliukozės.
Todėl laktozės sintetazė katalizuoja priešingą reakciją, nei katalizuoja lizocimas (kuris suskaido β-1,4 gliukozidinę jungtį)
Laktozės sintetazė yra dimeris, tai yra, ji sudaryta iš dviejų baltymų grandinių, kurių viena turi katalizines savybes ir yra panaši į lizocimo, o kita - reguliuojantis subvienetas.
Nėštumo metu glikoproteinus sintezuoja pieno liaukos ląstelės, veikdamos galatoziltransferazę (jos „sekos homologija 40% su lizocimu“): šis fermentas gali perkelti galaktozilo grupę iš didelės energijos struktūros į glikoproteinų struktūra.Nėštumo metu sukelia galaktoziltransferazę koduojančio geno išraiška (taip pat yra ir kitų genų, kurie taip pat suteikia kitų produktų): padidėja krūties dydis, nes aktyvuojama pieno liauka (anksčiau). neaktyvus), kuris turi gaminti pieną. Gimdymo metu gaminamas α-laktalbuminas, kuris yra reguliuojantis baltymas: jis gali reguliuoti galaktoziltransferazės katalizinį pajėgumą (diskriminuojant substratą). Galaktoziltransferazė, modifikuota α-laktalbuminu, gali perkelti galaktozilą į gliukozės molekulė: sudaro β-1,4 glikozidinį ryšį ir suteikia laktozės (laktozės sintetazės).
Taigi galaktozės transferazė paruošia pieno liauką prieš gimdymą ir gamina pieną po gimdymo.
Glikoproteinų gamybai galaktoziltransferazė jungiasi prie galaktozilo ir NAG; gimdymo metu laktazinis albuminas prisijungia prie galaktoziltransferazės, todėl pastaroji atpažįsta gliukozę ir nebeskiria laktozės.