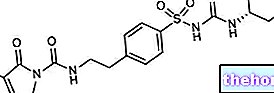
Veikliosios medžiagos: Prasugrel
Efient 10 mg plėvele dengtos tabletės
Efient 5 mg plėvele dengtos tabletės
Kodėl vartojamas Efient? Kam tai?
Efient, kurio sudėtyje yra veikliosios medžiagos prasugrelio, priklauso vaistų, vadinamų antitrombocitinėmis medžiagomis, grupei. Trombocitai yra labai mažos ląstelės, kurios cirkuliuoja kraujyje. Kai kraujagyslė yra pažeista, pavyzdžiui, jei ji yra supjaustyta, trombocitai susilieja ir prisideda prie kraujo krešulio (trombo) susidarymo. Todėl trombocitai yra būtini norint sustabdyti kraujavimą. Jei sukietėjusiose kraujagyslėse, pvz., Arterijoje, susidaro krešulių, jie gali būti labai pavojingi, nes gali užblokuoti kraujo tekėjimą ir sukelti širdies priepuolį (miokardo infarktą), insultą ar mirtį. Krešuliai arterijose, kuriais kraujas patenka į širdį, taip pat gali sumažinti kraujo tekėjimą į širdį ir sukelti nestabilią krūtinės anginą (stiprų krūtinės skausmą).
Efient slopina trombocitų agregaciją ir todėl sumažina kraujo krešulių susidarymo galimybę.
Efient buvo paskirtas Jums, nes anksčiau sirgote širdies priepuoliu ar nestabilia krūtinės angina ir buvote gydomas užblokuotų širdies arterijų atidarymo procedūra. Jums taip pat galėjo būti uždėtas vienas ar daugiau stentų į užblokuotą ar susiaurėjusią arteriją, kad būtų atkurta kraujotaka. „Efient“ sumažina tikimybę, kad patirsite kitą širdies priepuolį ar insultą arba mirsite dėl vieno iš šių aterotrombozinių reiškinių. Gydytojas taip pat paskirs acetilsalicilo rūgšties ( aspirinas), dar vienas antitrombocitinis vaistas.
Kontraindikacijos Kai Efient vartoti negalima
Efient vartoti negalima
- Jeigu yra alergija (padidėjęs jautrumas) prasugreliui arba bet kuriai pagalbinei Efient medžiagai. Alerginė reakcija gali būti atpažįstama, nes ji sukelia bėrimą, niežėjimą, veido patinimą, lūpų patinimą ar švokštimą.
- Jei sergate sveikatos sutrikimu, dėl kurio gali prasidėti kraujavimas, pvz., Kraujavimas iš skrandžio ar žarnyno.
- Jei anksčiau patyrėte insultą arba praeinantį išemijos priepuolį (TIA).
- Jei sergate sunkia kepenų liga.
Atsargumo priemonės Vartojant prieš Efient vartojimą
Jei atsiranda bet kuri iš toliau išvardytų situacijų, prieš pradėdami vartoti Efient pasakykite gydytojui:
- Jei yra padidėjusi kraujavimo rizika, pavyzdžiui:
- 75 metų ar vyresni. Gydytojas paskirs 5 mg paros dozę, nes vyresniems nei 75 metų pacientams padidėja kraujavimo rizika.
- neseniai patirta sunki trauma
- neseniai atlikta operacija (įskaitant kai kurias odontologines procedūras)
- neseniai ar pasikartojantis kraujavimas iš skrandžio ar žarnyno (pvz., skrandžio opa ar gaubtinės žarnos polipas)
- kūno svoris yra mažesnis nei 60 kg. Gydytojas paskirs 5 mg Efient paros dozę, jei sveriate mažiau nei 60 kg - vidutinio sunkumo kepenų ar inkstų liga.
- jeigu vartojate tam tikrų vaistų (žr. „Efient vartojimas su kitais vaistais“);
- jeigu per kitas septynias dienas planuojama atlikti planinę operaciją (įskaitant kai kurias odontologines procedūras). Gydytojas gali patarti laikinai nutraukti Efient vartojimą, nes padidėja kraujavimo rizika
- Jei kada nors buvo alerginių (padidėjusio jautrumo) reakcijų į klopidogrelį ar bet kurį kitą vaistą nuo trombocitų, prieš pradėdami vartoti Efient, pasakykite gydytojui. Jei pavartojote Efient ir pasireiškė alerginės reakcijos, kurios gali būti pripažintos „bėrimu, niežuliu, veido patinimu, lūpų patinimu ar dusuliu“, nedelsdami pasakykite gydytojui.
Vartojant Efient:
Nedelsdami pasakykite gydytojui, jei Jums pasireiškė sveikatos būklė, vadinama trombozine trombocitopenine purpura (PTT), įskaitant karščiavimą ir kraujosruvas po oda, kurios gali pasirodyti kaip maži raudoni taškeliai, su nepaaiškinamu giliu nuovargiu, sumišimu, spalvos pasikeitimu arba be jo. (gelta) (žr. 4 skyrių „Galimas šalutinis poveikis“).
Vaikai ir paaugliai
Efient neskirtas vaikams ir jaunesniems kaip 18 metų paaugliams.
Sąveika Kokie vaistai ar maistas gali pakeisti Efient poveikį
Pasakykite gydytojui, jei vartojate, neseniai vartojote arba galite vartoti kitų vaistų, įskaitant įsigytus be recepto, maisto papildus ir vaistažoles. Ypač svarbu pasakyti gydytojui, jei esate gydomas klopidogreliu (antitrombocitiniu vaistu), varfarinu (antikoaguliantu) arba „nesteroidiniais vaistais nuo uždegimo“ skausmui malšinti ir karščiavimui mažinti (pvz., Ibuprofenu, naproksenas, etorikoksibas). Vartojant kartu su Efient, šie vaistai gali padidinti kraujavimo riziką.
Vartodami kitus vaistus Efient vartokite tik tuo atveju, jei gydytojas nurodė.
Įspėjimai Svarbu žinoti, kad:
Nėštumas ir žindymo laikotarpis
Pasakykite gydytojui, jei esate nėščia ar planuojate pastoti, kol vartojate Efient. Efient galite vartoti tik pasitarę su gydytoju apie galimą naudą ir galimą riziką negimusiam vaikui.
Jei žindote kūdikį, prieš pradėdami vartoti bet kokį vaistą, pasitarkite su gydytoju arba vaistininku
Vairavimas ir mechanizmų valdymas
Mažai tikėtina, kad Efient paveiks jūsų gebėjimą vairuoti ar valdyti mechanizmus.
Efient sudėtyje yra laktozės.
Jei gydytojas Jums yra sakęs, kad netoleruojate kokių nors angliavandenių, prieš vartodami šį vaistą pasitarkite su gydytoju.
Dozė, vartojimo būdas ir laikas Kaip vartoti Efient: Dozavimas
Efient visada vartokite tiksliai, kaip nurodė gydytojas. Jei abejojate, pasitarkite su gydytoju arba vaistininku.
Įprasta Efient dozė yra 10 mg per parą. Gydymas prasidės vienkartine 60 mg doze. Jei jūsų kūno svoris yra mažesnis nei 60 kg arba esate vyresnis nei 75 metų, Efient dozė yra 5 mg per parą.
Gydytojas taip pat lieps vartoti acetilsalicilo rūgštį - tiksliai nurodys, kokią dozę reikia gerti (paprastai nuo 75 mg iki 325 mg per parą).
Efient galite vartoti valgant arba nevalgius. Efient vartokite kiekvieną dieną maždaug tuo pačiu laiku. Nesmulkinkite ir nesulaužykite tabletės.
Svarbu pasakyti gydytojui, vaistininkui ir odontologui, kad vartojate Efient.
Perdozavimas Ką daryti pavartojus per didelę Efient dozę
Pavartojus per didelę Efient dozę
Nedelsdami kreipkitės į savo gydytoją arba artimiausią ligoninę, nes gali padidėti kraujavimas. Parodykite gydytojui Efient pakuotę.
Pamiršus pavartoti Efient
Jei pamiršote išgerti dozę, išgerkite vieną tabletę, kai tik pastebėsite. Jei pamiršote išgerti dozę visą dieną, kitą dieną išgerkite įprastą Efient dozę. Nevartokite dviejų dozių tą pačią dieną. Pakuotėse, kuriose yra 14, 28, 56, 84 ir 98 tabletės, paskutinės Efient tabletės išgėrimo dieną galite patikrinti ant lizdinės plokštelės išspausdinto kalendoriaus.
Nustojus vartoti Efient
Nenutraukite Efient vartojimo nepasitarę su gydytoju Jei nutrauksite Efient vartojimą per anksti, miokardo infarkto rizika gali būti didesnė.
Jeigu kiltų daugiau klausimų dėl šio vaisto vartojimo, kreipkitės į gydytoją arba vaistininką.
Šalutinis poveikis Koks yra Efient šalutinis poveikis
Efient, kaip ir visi kiti vaistai, gali sukelti šalutinį poveikį, nors jis pasireiškia ne visiems žmonėms.
Jei pastebėjote bet kurį iš šių šalutinių poveikių, nedelsdami kreipkitės į gydytoją:
- Staigus mieguistumas ar silpnumas rankoje, kojoje ar veide, ypač jei jie yra tik vienoje kūno pusėje
- Staigus sumišimas, sunku kalbėti ar suprasti, ką kiti sako
- Staigus vaikščiojimo sunkumas arba pusiausvyros ar koordinacijos praradimas
- Staigus galvos svaigimas ar staigus stiprus galvos skausmas be žinomos priežasties.
Visa tai gali būti insulto požymiai. Insultas yra nedažnas Efient šalutinis poveikis pacientams, kurie niekada nebuvo patyrę insulto ar trumpalaikio išeminio priepuolio (TIA).
Taip pat nedelsdami kreipkitės į gydytoją, jei pastebėjote bet kurį iš šių šalutinių poveikių:
- karščiavimas ir kraujosruvos po oda, kurios gali pasirodyti kaip labai maži raudoni taškeliai su nepaaiškinamu giliu nuovargiu, sumišimu, odos ar akių pageltimu (gelta) arba be jos (žr. 2 skyrių „KAS ŽINOTINA PRIEŠ VARTOJANT EFIENT“)
- „odos bėrimas, niežulys ar veido patinimas, lūpų / liežuvio patinimas ar švokštimas. Visa tai gali būti sunkios alerginės reakcijos požymiai (žr. 2 skyrių„ Kas žinotina prieš vartojant Efient “).
Jei pastebėjote bet kurį iš šių šalutinių poveikių, nedelsdami kreipkitės į gydytoją:
- Kraujas šlapime
- Kraujavimas iš tiesiosios žarnos, kraujas išmatose arba juodos spalvos išmatos
- Nekontroliuojamas kraujavimas, pavyzdžiui, nuo pjūvio
Visa tai gali būti kraujavimo požymiai, dažniausiai pasitaikantis Efient šalutinis poveikis. Nors retas, sunkus kraujavimas gali būti pavojingas gyvybei.
Dažnas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 10 žmonių)
- Kraujavimas iš skrandžio ar žarnyno
- Kraujavimas iš adatos dūrio vietos
- Kraujavimas iš nosies
- Odos bėrimas
- Mažos raudonos mėlynės ant odos (mėlynės)
- Kraujas šlapime
- Hematoma (kraujavimas po oda injekcijos vietoje arba į raumenis, sukeliantis patinimą)
- Mažas hemoglobino kiekis arba mažas raudonųjų kraujo kūnelių skaičius (anemija)
- Sumušimai
Nedažnas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 100 žmonių)
- Alerginė reakcija (bėrimas, niežėjimas, lūpų / liežuvio patinimas ar dusulys)
- Savaiminis kraujavimas iš akies, tiesiosios žarnos, dantenų ar pilvo aplink vidaus organus
- Kraujavimas po operacijos
- Kosulys krauju
- Kraujas išmatose
Retas šalutinis poveikis (gali pasireikšti ne daugiau kaip 1 iš 1 000 žmonių)
- Mažas trombocitų kiekis kraujyje
- Poodinė hematoma (kraujavimas po oda, sukeliantis patinimą)
Pranešimas apie šalutinį poveikį
Jeigu pasireiškė sunkus šalutinis poveikis arba pastebėjote šiame lapelyje nenurodytą šalutinį poveikį, pasakykite gydytojui arba vaistininkui. Apie šalutinį poveikį taip pat galite pranešti tiesiogiai naudodamiesi V priede nurodyta nacionaline pranešimo sistema. Pranešdami apie šalutinį poveikį galite padėti gauti daugiau informacijos apie šio vaisto saugumą.
Galiojimo laikas ir išlaikymas
Laikykite Efient vaikams nepastebimoje ir nepasiekiamoje vietoje.
Ant lizdinės plokštelės ir dėžutės po „Tinka iki“ nurodytam tinkamumo laikui pasibaigus, Efient vartoti negalima. Vaistas tinkamas vartoti iki paskutinės mėnesio dienos.
Laikyti gamintojo pakuotėje, kad vaistas būtų apsaugotas nuo oro ir drėgmės.
Vaistų negalima išmesti į kanalizaciją ar buitines atliekas. Paklauskite vaistininko, kaip išmesti nebenaudojamus vaistus. Tai padės apsaugoti aplinką.
Efient sudėtis
- Veiklioji medžiaga yra prasugrelis.
Efient 10 mg: kiekvienoje tabletėje yra 10 mg prasugrelio (hidrochlorido pavidalu).
Efient 5 mg: kiekvienoje tabletėje yra 5 mg prasugrelio (hidrochlorido pavidalu).
- Pagalbinės medžiagos yra mikrokristalinė celiuliozė, manitolis (E421), natrio kroskarmeliozė, hipromeliozė (E464), magnio stearatas, laktozės monohidratas, titano dioksidas (E171), triacetinas (E1518), raudonasis geležies oksidas (tik 10 mg tabletėms) (E172) , geltonasis geležies oksidas (E172) ir talkas.
Efient išvaizda ir kiekis pakuotėje
Efient 10 mg: tabletės yra smėlio spalvos ir dvigubos rodyklės formos, vienoje pusėje įspausta „10 MG“, kitoje - „4759“.
Efient 5 mg: tabletės yra geltonos ir dvigubos rodyklės formos, vienoje pusėje įspausta „5 MG“, kitoje - „4760“.
Efient tiekiamas pakuotėmis po 14, 28, 30, 56, 84, 90 ir 98 tabletes.
Gali būti tiekiamos ne visų dydžių pakuotės.
Šaltinio pakuotės lapelis: AIFA (Italijos vaistų agentūra). Turinys paskelbtas 2016 m. Sausio mėn. Pateikta informacija gali būti neatnaujinta.
Norint pasiekti naujausią versiją, patartina apsilankyti AIFA (Italijos vaistų agentūra) svetainėje. Atsisakymas ir naudinga informacija.
01.0 VAISTINIO PREPARATO PAVADINIMAS
EFIENT 10 MG TABLETĖS, Dengtos plėvele
02.0 KOKYBINĖ IR KIEKYBINĖ SUDĖTIS
Kiekvienoje tabletėje yra 10 mg prasugrelio (hidrochlorido pavidalu).
Pagalbinės medžiagos, kurių poveikis žinomas: kiekvienoje tabletėje yra 2,1 mg laktozės.
Išsamų pagalbinių medžiagų sąrašą žr. 6.1 skyriuje.
03.0 FARMACINĖ FORMA
Plėvele dengta tabletė (tabletė).
Smėlio spalvos, dvigubos rodyklės formos tabletės, kurių vienoje pusėje įspausta „10 MG“, o kitoje - „4759“.
04.0 KLINIKINĖ INFORMACIJA
04.1 Terapinės indikacijos
Efient, vartojamas kartu su acetilsalicilo rūgštimi (ASA), skirtas aterotrombozinių reiškinių profilaktikai suaugusiems pacientams, sergantiems ūminiu koronariniu sindromu (AKS) (t. Y. Nestabili krūtinės angina, miokardo infarktas be ST segmento pakilimo [UA / NSTEMI] arba ST segmentas) padidėjęs miokardo infarktas [STEMI]), kuriam atliekama pirminė arba uždelsta perkutaninė koronarinė intervencija (PKI).
Daugiau informacijos rasite 5.1 skyriuje.
04.2 Dozavimas ir vartojimo metodas
Dozavimas
Suaugusieji
Efient reikia pradėti nuo vienos 60 mg įsotinamosios dozės, o po to tęsti 10 mg kartą per parą. Pacientai, vartojantys Efient, taip pat turi vartoti 75–325 mg acetilsalicilo rūgšties (ASS) per parą.
Pacientams, sergantiems ūminiu koronariniu sindromu (AKS), kuriems atliekama perkutaninė koronarinė intervencija, anksti nutraukus bet kokio antitrombocitinio vaisto, įskaitant Efient, vartojimą, gali padidėti trombozės, miokardo infarkto ar mirties rizika dėl paciento sveikatos būklės. rekomenduojama vartoti mėnesius, nebent Efient vartojimo nutraukimas yra kliniškai pagrįstas (žr. 4.4 ir 5.1 skyrius).
Amžiaus pacientai ≥ 75 metai
Efient vartoti vyresniems kaip 75 metų pacientams apskritai nerekomenduojama. Jei paskyręs gydytojas, atidžiai įvertinęs individualų naudos ir rizikos santykį (žr. 4.4 skyrių), manoma, kad Efient gydyti būtina šios amžiaus grupės pacientams ≥ 75 metų, po 60 mg įsotinamosios dozės reikia skirti mažesnę palaikomąją 5 mg dozę. ≥ 75 metų pacientams padidėjęs jautrumas kraujavimui ir padidėjusi veikliosios prasugrelio medžiagos metabolito ekspozicija (žr. 4.4, 4.8, 5.1 ir 5.2).
Pacientai, kurių kūno svoris
Efient reikia vartoti vieną 60 mg įsotinamąją dozę, po to 5 mg vieną kartą per parą. Palaikomoji 10 mg dozė nerekomenduojama. Taip yra dėl to, kad padidėja veiklaus prasugrelio metabolito ekspozicija ir padidėja kraujavimo rizika pacientams, turintiems svorio.
Inkstų funkcijos sutrikimas
Pacientams, sergantiems inkstų nepakankamumu, įskaitant pacientus, kuriems yra galutinė inkstų liga, dozės koreguoti nereikia (žr. 5.2 skyrių). Terapinės patirties pacientams, sergantiems inkstų nepakankamumu, yra nedaug (žr. 4.4 skyrių).
Kepenų funkcijos sutrikimas
Pacientams, kuriems yra lengvas ar vidutinio sunkumo kepenų funkcijos sutrikimas (A ir B klasė pagal Child-Pugh), dozės koreguoti nereikia (žr. 5.2 skyrių). Pacientų, kuriems yra lengvas ar vidutinio sunkumo kepenų funkcijos sutrikimas, gydymo patirties yra nedaug (žr. 4.4 skyrių). Efient draudžiama vartoti pacientams, kuriems yra sunkus kepenų funkcijos sutrikimas (C klasė pagal Child Pugh).
Vaikų populiacija
Efient saugumas ir veiksmingumas jaunesniems kaip 18 metų vaikams dar neištirti, duomenų nėra.
Vartojimo metodas
Vartoti per burną. Efient galima vartoti neatsižvelgiant į maistą.Skyrus 60 mg prasugrelio prisotinamosios dozės nevalgius, vaistinis preparatas gali veikti greičiau (žr. 5.2 skyrių). Negalima sutraiškyti ar sulaužyti tabletės.
04.3 Kontraindikacijos
Padidėjęs jautrumas veikliajai arba bet kuriai 6.1 skyriuje nurodytai pagalbinei medžiagai.
Vyksta patologinis kraujavimas.
Insultas ar praeinantis išeminis priepuolis (TIA).
Sunkus kepenų funkcijos sutrikimas (C klasės pagal Child-Pugh).
04.4 Specialūs įspėjimai ir tinkamos atsargumo priemonės
Kraujavimo rizika
3 fazės klinikinio tyrimo metu pagrindiniai išskyrimo kriterijai buvo padidėjusi kraujavimo rizika; anemija; trombocitopenija; atradimų, rodančių intrakranijinę patologiją, istorija.
Pacientams, sergantiems ūminiu koronariniu sindromu, kuriems buvo atlikta perkutaninė vainikinių arterijų intervencija, gydomi Efient ir ASA, padidėjusi didelio ir nedidelio kraujavimo rizika pagal TIMI klasifikavimo sistemą.
Todėl Efient vartojimą pacientams, kuriems yra padidėjusi kraujavimo rizika, reikia apsvarstyti tik tada, kai manoma, kad nauda išemijos prevencijos atžvilgiu yra didesnė už sunkaus kraujavimo riziką. Ši atsargumo priemonė ypač taikoma pacientams:
• ≥ 75 metų amžiaus (žr. Toliau).
• turintis polinkį kraujuoti (pvz., Dėl neseniai patirtos traumos, neseniai atliktos operacijos, neseniai įvykusio ar pasikartojančio kraujavimo iš virškinimo trakto ar besitęsiančios pepsinės opos ligos);
• su kūno svoriu
• kartu vartojant vaistus, galinčius padidinti kraujavimo riziką, įskaitant geriamuosius antikoaguliantus, klopidogrelį, nesteroidinius vaistus nuo uždegimo (NVNU) ir fibrinolitikus.
Pacientams, kuriems kraujavimas tebesitęsia ir kuriems reikia pakeisti farmakologinį Efient poveikį, gali prireikti perpilti trombocitus.
Efient paprastai nerekomenduojama skirti vyresniems kaip 75 metų pacientams ir jį reikia daryti atsargiai, kai „gydytojas, atidžiai įvertinęs individualią naudos ir rizikos santykį, rodo, kad išeminių įvykių prevencinė nauda yra didesnė už rimto kraujavimo riziką“. . 3 fazės klinikinio tyrimo metu šiems pacientams buvo didesnė kraujavimo rizika, įskaitant mirtiną kraujavimą, palyginti su amžiaus pacientais
Gydymo prasugreliu patirties pacientams, kurių inkstų funkcija sutrikusi (įskaitant pacientus, sergančius galutinės stadijos inkstų liga (ESRD)), ir pacientams, kuriems yra vidutinio sunkumo kepenų funkcijos sutrikimas, yra nedaug. Šiems pacientams gali padidėti kraujavimo rizika.
Todėl šiems pacientams prasugrelį reikia vartoti atsargiai.
Pacientus reikia įspėti, kad vartojant prasugrelį (kartu su ASS) kraujavimas gali sustoti ilgiau nei įprasta, ir apie bet kokį neįprastą kraujavimą (pagal vietą ar trukmę) informuoti gydytoją.
Chirurginė intervencija
Prieš atlikdami bet kokią operaciją ir prieš pradėdami vartoti naują vaistą, pacientai turėtų pasakyti gydytojams ir odontologams, kad vartoja prasugrelį. Jei pacientui bus atliekama planinė operacija ir antitrombocitinis poveikis nėra tinkamas, Efient vartojimą reikia nutraukti likus ne mažiau kaip 7 dienoms iki operacijos. Pacientams, kuriems atliekama CABG operacija, kraujavimas gali padažnėti (3 kartus). 7 dienos nutraukti prasugrelio vartojimą (žr. 4.8 skyrių). Prasugrelio naudą ir riziką reikia atidžiai apsvarstyti tiems pacientams, kurių koronarinė anatomija nenustatyta, ir galima skubi CABG operacija.
Padidėjęs jautrumas, įskaitant angioedemą
Pranešta apie padidėjusio jautrumo reakcijas, įskaitant angioneurozinę edemą pacientams, vartojantiems prasugrelį, įskaitant pacientus, kuriems anksčiau buvo padidėjusio jautrumo reakcijų klopidogreliui. Pacientams, kuriems anksčiau buvo alergija tienopiridinams, patariama stebėti padidėjusio jautrumo požymius (žr. 4.8 skyrių).
Trombozinė trombocitopeninė purpura (PTT)
Pranešta apie PTT vartojant prasugrelį. PTT yra rimta būklė, kurią reikia nedelsiant gydyti.
Laktozė
Pacientams, kuriems nustatytas retas paveldimas sutrikimas-galaktozės netoleravimas, Lapp laktazės trūkumas arba gliukozės ir galaktozės malabsorbcija, Efient vartoti negalima..
04.5 Sąveika su kitais vaistiniais preparatais ir kitos sąveikos formos
Varfarinas: Efient ir kitų kumarino darinių, išskyrus varfariną, vartojimas nebuvo tirtas. Kadangi gali padidėti kraujavimo rizika, atsargiai reikia vartoti kartu varfariną (ar kitus kumarino darinius) ir prasugrelį (žr. 4.4 skyrių).
Nesteroidiniai vaistai nuo uždegimo (NVNU):
Kartu vartojamas lėtinis NVNU netirtas. Kadangi gali padidėti kraujavimo rizika, lėtinius NVNU (įskaitant COX-2 inhibitorius) ir Efient reikia skirti atsargiai (žr. 4.4 skyrių).
Efient galima vartoti kartu su vaistiniais preparatais, kuriuos metabolizuoja citochromo P450 fermentai (įskaitant statinus), arba vaistiniais preparatais, kurie yra citochromo P450 fermentų induktoriai ar inhibitoriai. Efient taip pat galima vartoti kartu su ASH, heparinu, digoksinu ir vaistais, kurie padidina skrandžio pH, įskaitant protonų siurblio inhibitorius ir H2 blokatorius.
Nors Efient nebuvo specifinių sąveikos tyrimų objektas, 3 fazės klinikinio tyrimo metu jis buvo skiriamas kartu su mažos molekulinės masės heparinu, bivalirudinu ir GP IIb / IIIa inhibitoriais (informacijos apie GP IIb / IIIa inhibitoriaus tipą nėra). nebuvo kliniškai reikšmingos nepageidaujamos sąveikos požymių.
Kitų vaistinių preparatų poveikis Efient:
Acetilsalicilo rūgštis: Efient reikia vartoti kartu su ASS. Nors galima farmakodinaminė sąveika su ASS ir dėl to padidėjusi kraujavimo rizika, prasugrelio veiksmingumo ir saugumo įrodymai pateikiami pacientams, gydomiems kartu su ASS.
Heparinas: Viena nefrakcionuoto heparino intraveninė boliuso dozė (100 V / kg) reikšmingai nepakeitė prasugrelio sukeltos trombocitų agregacijos slopinimo. Panašiai prasugrelis reikšmingai nepakeitė heparino poveikio krešėjimo parametrams.
Todėl abu vaistus galima vartoti kartu. Vartojant Efient kartu su heparinu, gali padidėti kraujavimo rizika.
Statinai: Atorvastatinas (80 mg per parą) nepakeitė prasugrelio farmakodinaminio aktyvumo ar jo trombocitų agregacijos slopinimo. Todėl manoma, kad CYP3A substrato statinai neturės įtakos prasugrelio farmakokinetikai ar trombocitų agregacijos slopinimui..
Vaistai, didinantys skrandžio pH: Kartu vartojant ranitidiną (H2 blokatorių) arba lansoprazolą (protonų siurblio inhibitorių) kasdien, aktyviojo prasugrelio metabolito AUC ir Tmax nepasikeitė, tačiau Cmax sumažėjo 14% ir 29%. , Efient buvo skiriamas nepriklausomai nuo to, ar kartu buvo skiriamas protonų siurblio inhibitorius ar H2 blokatorius. 60 mg prisotinamosios prasugrelio dozės vartojimas kartu nevartojant protonų siurblio inhibitorių. Tai gali sukelti greitesnį vaisto veikimo pradžią.
CYP3A inhibitoriaiKetokonazolas (400 mg per parą), stiprus ir selektyvus CYP3A4 ir CYP3A5 inhibitorius, nepakeitė prasugrelio sukeltos trombocitų agregacijos slopinimo ar aktyvaus prasugrelio metabolito AUC ir T, tačiau sumažino Cmax 34% iki 46% Todėl CYP3A inhibitoriai, tokie kaip priešgrybeliniai azolo preparatai, ŽIV proteazės inhibitoriai, klaritromicinas, telitromicinas, verapamilis, diltiazemas, indinaviras, ciprofloksacinas ir greipfrutų sultys, manoma, neturės reikšmingo poveikio aktyvaus metabolito farmakokinetikai.
Citochromo P450 induktoriai: Rifampicinas (600 mg per parą), stiprus CYP3A ir CYP2B6 induktorius, taip pat CYP2C9, CYP2C19 ir CYP2C8 induktorius, reikšmingai nepakeitė prasugrelio farmakokinetikos. Todėl manoma, kad žinomi CYP3A induktoriai, tokie kaip rifampicinas, karbamazepinas ir kiti citochromo P450 induktoriai, neturės reikšmingo poveikio aktyvaus metabolito farmakokinetikai.
Efient poveikis kitiems vaistiniams preparatams:
Digoksinas: Prasugrelis kliniškai reikšmingo poveikio digoksino farmakokinetikai neturi.
Vaistai, kuriuos metabolizuoja CYP2C9Prasugrelis neslopino CYP2C9, nes neturėjo įtakos varfarino-S farmakokinetikai. Kadangi gali padidėti kraujavimo rizika, atsargiai reikia vartoti varfariną ir Efient kartu (žr. 4.4 skyrių).
Vaistai, kuriuos metabolizuoja CYP2B6Prasugrelis yra silpnas CYP2B6 inhibitorius. Sveikiems asmenims prasugrelis 23%sumažino hidroksibupropiono, CYP2B6 tarpininkaujamo bupropiono metabolito, poveikį. Šis poveikis gali būti kliniškai svarbus tik tada, kai prasugrelis vartojamas kartu su vaistiniais preparatais, kurių vienintelis metabolizmo kelias yra CYP2B6 ir kurių terapinis langas yra ribotas (pvz., Ciklofosfamidas, efavirenzas).
04.6 Nėštumas ir žindymo laikotarpis
Nėščioms ir žindančioms moterims klinikinių tyrimų neatlikta.
Nėštumas
Tyrimai su gyvūnais nerodo tiesioginio žalingo poveikio nėštumui, embriono / vaisiaus vystymuisi, gimdymui ar pogimdyminiam vystymuisi (žr. 5.3 skyrių). Kadangi reprodukcijos tyrimai su gyvūnais ne visada prognozuoja poveikį žmonėms, Efient nėštumo metu galima vartoti tik tuo atveju, jei galima nauda pateisina galimą pavojų vaisiui.
Maitinimo laikas
Nežinoma, ar prasugrelis išsiskiria į motinos pieną. Tyrimai su gyvūnais parodė, kad prasugrelis patenka į motinos pieną, todėl žindymo laikotarpiu prasugrelio vartoti nerekomenduojama.
Vaisingumas
Prasugrelis neturėjo įtakos žiurkių patinų ir patelių vaisingumui, kai jiems buvo skiriama geriamoji dozė iki 240 kartų didesnė už rekomenduojamą palaikomąją paros dozę (apskaičiuotą mg / m2).
04.7 Poveikis gebėjimui vairuoti ir valdyti mechanizmus
Manoma, kad Prasugrel neveiks gebėjimo vairuoti ir valdyti mechanizmus arba nežymiai.
04.8 Nepageidaujamas poveikis
Saugos profilio santrauka
Saugumas pacientams, sergantiems ūminiu koronariniu sindromu, kuriems atliekama perkutaninė koronarinė intervencija, buvo įvertintas klopidogrelio (TRITON) kontroliuojamame klinikiniame tyrime, kurio metu 6 741 pacientas buvo gydomas prasugreliu (60 mg įsotinamoji dozė ir palaikomoji 10 mg paros dozė). vidutiniškai 14,5 mėnesio (5 802 pacientai buvo gydomi ilgiau nei 6 mėnesius, 4 136 pacientai buvo gydomi ilgiau nei 1 metus). Tiriamųjų vaistų nutraukimo dažnis dėl nepageidaujamų reiškinių buvo 7,2% prasugrelio ir 6,3% klopidogrelio. Iš jų kraujavimas buvo dažniausia nepageidaujama reakcija, dėl kurios buvo nutrauktas abiejų vaistų tiriamasis gydymas (2,5% prasugrelio ir 1,4% klopidogrelio).
Kraujavimas
Kraujavimas, nesusijęs su vainikinių arterijų šuntavimu (CABG)
TRITON tyrimo metu pacientų, kuriems pasireiškė kraujavimo epizodas, nesusijęs su vainikinių arterijų šuntavimo operacija (CABG), dažnis parodytas 1 lentelėje. Didelio kraujavimo (pagal TIMI apibrėžimus) dažnis, nesusijęs su vainikinių arterijų šuntavimu (CABG), įskaitant tie, kuriems gresia mirtis ir mirtini pavojai, taip pat nedidelis kraujavimas (pagal TIMI apibrėžimus) buvo statistiškai reikšmingai didesnis prasugreliu gydytiems asmenims, palyginti su klopidogreliu gydomais asmenimis tiek UA / NSTEMI, nei visoje AKS populiacijoje . STEMI populiacijoje reikšmingų skirtumų nepastebėta. Dažniausia savaiminio kraujavimo vieta buvo virškinimo traktas (1,7% vartojant prasugrelį ir 1,3% vartojant klopidogrelį); dažniausia kraujavimo vieta buvo arterinė prieiga (1,3% vartojant prasugrelį ir 1,2% vartojant klopidogrelį).
1 lentelė. Kraujavimo dažnis, nesusijęs su vainikinių arterijų šuntavimo operacija (CABG) a (% pacientų)
a Įvykiai, apibrėžiami tiriamosios miokardo infarkto trombolizės tyrimo grupės (TIMI) kriterijais centralizuotas.
b Kiti standartiniai gydymo būdai buvo skirti atitinkamai.
c Bet koks intrakranijinis kraujavimas arba bet koks kliniškai akivaizdus kraujavimas, susijęs su sumažėjimu hemoglobino ≥5 g / dl.
d Kraujavimas esant mirties rizikai yra didelio kraujavimo pogrupis (pagal TIMI apibrėžimus) e apima toliau išvardytus tipus. Pacientus galima suskaičiuoti daugiau nei vienoje eilėje.
ir ICH = intrakranijinis kraujavimas.
f Kliniškai akivaizdus kraujavimas, susijęs su hemoglobino sumažėjimu ≥3 g / dl, bet
Amžiaus pacientai ≥ 75 metai
Didelio ar nedidelio kraujavimo (TIMI) dažnis, nesusijęs su vainikinių arterijų šuntavimo operacija (CABG):
* TRITON tyrimas su AKS sergančiais pacientais, kuriems atliekama PCI
** TRILOGY-ACS tyrimas su pacientais, kuriems neatliekama PCI (žr. 5.1 skyrių):
į 10 mg prasugrelio; prasugrelio 5 mg, jei
Pacientai, kurių kūno svoris
Didelio ar nedidelio kraujavimo (TIMI) dažnis, nesusijęs su vainikinių arterijų šuntavimo operacija (CABG):
* TRITON tyrimas su AKS sergančiais pacientais, kuriems atliekama PCI
** TRILOGY-ACS tyrimas su pacientais, kuriems neatliekama PCI (žr. 5.1 skyrių):
į 10 mg prasugrelio; prasugrelio 5 mg, jei ≥ 75 metų
Pacientai, sveriantys ≥60 kg ir vyresni
Pacientams, sveriantiems ≥60 kg ir amžiaus
Kraujavimas, susijęs su vainikinių arterijų šuntavimu (CABG)
3 fazės klinikinio tyrimo metu 437 pacientams buvo atlikta vainikinių arterijų šuntavimo operacija (CABG). Iš šių pacientų didelio ar nedidelio kraujavimo (TIMI) dažnis, susijęs su vainikinių arterijų šuntavimo operacija (CABG), buvo 14,1% prasugrelio grupės ir 4,5% klopidogrelio grupės. Didžiausia kraujavimo epizodų rizika tiriamiesiems, gydytiems prasugreliu, išliko iki 7 dienų po paskutinės tiriamojo vaisto dozės. Pacientams, kurie gavo tienopiridiną per 3 dienas iki vainikinių arterijų šuntavimo (CABG), didelio ar nedidelio kraujavimo dažnis (TIMI) buvo 26,7% (12 iš 45 pacientų) prasugrelio grupėje, palyginti su 5,0% (3 iš 60 pacientų) klopidogrelio grupėje. Pacientams, kurie paskutinę tienopiridino dozę gavo per 4–7 dienas iki vainikinių arterijų šuntavimo (CABG), dažnis prasugrelio grupėje sumažėjo iki 11,3% (9 iš 80 pacientų) ir 3,4 % (3 iš 89 pacientų) klopidogrelio grupėje. Praėjus daugiau nei 7 dienoms po vaisto vartojimo nutraukimo, pastebėtas kraujavimas, susijęs su vainikinių arterijų šuntavimo operacija (CABG), abiejose gydymo grupėse buvo panašus (žr. 4.4 skyrių).
Nepageidaujamų reakcijų santrauka
2 lentelėje apibendrintos hemoraginės ir nehemoraginės nepageidaujamos reakcijos TRITON tyrimo metu arba spontaniškos ataskaitos, suskirstytos pagal dažnį ir sistemas bei organus. Jų dažnis apibrėžiamas taip: Labai dažni (≥ 1/10); dažni (≥ 1/100,
2 lentelė: hemoraginės ir nehemoraginės nepageidaujamos reakcijos
Pacientams, kuriems praeityje buvo išeminis priepuolis (TIA) arba insultas arba jų nebuvo, 3 fazės tyrimo metu insulto dažnis buvo toks (žr. 4.4 skyrių):
* ICH = intrakranijinis kraujavimas.
Pranešimas apie įtariamas nepageidaujamas reakcijas
Svarbu pranešti apie įtariamas nepageidaujamas reakcijas, atsiradusias po vaistinio preparato registravimo, nes tai leidžia nuolat stebėti vaisto naudos ir rizikos santykį. Sveikatos priežiūros specialistų prašoma pranešti apie bet kokias įtariamas nepageidaujamas reakcijas per nacionalinę pranešimo sistemą. .
04.9 Perdozavimas
Perdozavus Efient, gali pailgėti kraujavimo laikas ir atsirasti kraujavimo komplikacijų. Nėra informacijos apie prasugrelio farmakologinio aktyvumo „atšaukimą“; tačiau kai reikia greitai ištaisyti pailgėjusį kraujavimo laiką, galima apsvarstyti trombocitų ar kitų kraujo produktų perpylimą.
05.0 FARMAKOLOGINĖS SAVYBĖS
05.1 Farmakodinaminės savybės
Farmakoterapinė grupė - antitrombocitiniai vaistai, išskyrus hepariną.
ATC kodas: B01AC22.
Farmakodinaminis poveikis
Prasugrelis yra trombocitų aktyvacijos ir agregacijos inhibitorius, kuris negrįžtamai jungiasi prie aktyvaus metabolito prie P2Y12 klasės ADP trombocitų receptorių. Trombocitų funkcija gali sumažinti širdies ir kraujagyslių sistemos sutrikimų, tokių kaip mirtis, miokardo infarktas ar insultas, dažnį.
Išgėrus 60 mg prasugrelio dozę, ADP sukeltas trombocitų agregacijos slopinimas pasireiškia 15 minučių, kai vartojama 5 mcM ADP, o 30 minučių-20 mcM ADP. % su 5 mcM ADP ir 79% su 20 mcM ADP, abiem atvejais 89% sveikų asmenų ir pacientų, sergančių stabilia ateroskleroze, per 1 valandą pasiekė mažiausiai 50% trombocitų agregacijos slopinimo. Trombocitų agregacijos slopinimas, pasiektas vartojant Prasugrel, rodo mažesnį (9%) ir individualų (12%) kintamumą tiek 5 mcM, tiek 20 mcM ADP.Vidutinis trombocitų agregacijos slopinimas esant pusiausvyrai buvo atitinkamai 74% ir 69%, atitinkamai 5 mcM ADP ir 20 mcM ADP, ir buvo pasiektas praėjus 3–5 dienoms po vienkartinės dozės vartojimo. mg prasugrelio, prieš tai buvo skiriama 60 mg įsotinamoji dozė. Daugiau kaip 98% tiriamųjų ≥ 20% slopino trombocitų agregaciją palaikomosios dozės metu.
Po gydymo trombocitų agregacija palaipsniui grįžo į pradinę vertę per 7–9 dienas po vienkartinės 60 mg pradinės prasugrelio dozės vartojimo ir per 5 dienas po to, kai buvo nutraukta palaikomoji pusiausvyra.
Duomenys apie perėjimą nuo klopidogrelio prie prasugrelio: 10 dienų išgėrus 75 mg klopidogrelio vieną kartą per parą, 40 sveikų asmenų buvo pereita prie 10 mg prasugrelio vieną kartą per parą, su 60 mg įsotinamąja doze arba be jos. Panašus ar didesnis trombocitų agregacijos slopinimas buvo pastebėtas vartojant prasugrelį. Tiesiogiai pereinant prie 60 mg prasugrelio įsotinamosios dozės, greičiau atsirado didesnis trombocitų slopinimas. Suleidus prisotinamąją 900 mg klopidogrelio dozę (kartu su ASS) 56 pacientai, sergantys AKS, 14 dienų buvo gydomi 10 mg prasugrelio vieną kartą per parą arba 150 mg klopidogrelio vieną kartą per parą, po to gydymas buvo pakeistas į atitinkamai 150 mg arba 10 mg prasugrelio klopidogrelį dar 14 dienų („perėjimas“). didžiausias trombocitų agregacijos slopinimas buvo pastebėtas pacientams, pakeitusiems 10 mg prasugrelio, palyginti su pacientais, gydytais 150 mg klopidogreliu. Tyrime, kuriame dalyvavo 276 pacientai, sergantys AKS, kuriems buvo atlikta PKI, buvo pakeista pradinė 600 mg klopidogrelio ar placebo dozė, skiriama paguldžius į ligoninę prieš koronarinę angiografiją, į 60 mg prasugrelio sotinamąją dozę. PKI sukėlė panašų trombocitų agregacijos slopinimo padidėjimą per 72 valandų tyrimo trukmę.
Veiksmingumas ir saugumas sergant ūminiu koronariniu sindromu
Trečiojo fazės TRITON tyrimo metu Efient (prasugrelis) buvo lyginamas su klopidogreliu, vartojamu kartu su ASS ir kitais standartiniais gydymo būdais. TRITON yra tarptautinis, atsitiktinių imčių, dvigubai aklas, lygiagrečios grupės daugiacentris tyrimas, kuriame dalyvavo 13 608 pacientai. Pacientai sirgo AKS su vidutinės ar didelės rizikos UA ir NSTEMI ar STEMI ir buvo gydomi PCI.
Pacientai, sergantys UA / NSTEMI per 72 valandas nuo simptomų atsiradimo arba su STEMI nuo 12 valandų iki 14 dienų nuo simptomų atsiradimo, buvo atsitiktinai atrinkti, žinant koronarinės kraujotakos anatomiją. Pacientai, sergantys STEMI per 12 valandų nuo simptomų pradžios ir suplanuoti pirminę PKI Visiems pacientams įsotinamoji dozė gali būti skiriama bet kuriuo metu nuo atsitiktinės atrankos iki 1 valandos po to, kai pacientas palieka laboratoriją, kurioje buvo atlikta širdies kateterizacija.
Pacientai, atsitiktinai atrinkti į prasugrelį (60 mg įsotinamoji dozė, po to 10 mg vieną kartą per parą) arba klopidogrelį (300 mg įsotinamoji dozė, po to 75 mg vieną kartą per parą), buvo gydomi vidutiniškai 14,5 mėnesio (ne ilgiau kaip 15 mėnesių, mažiausiai) 6 mėnesių stebėjimas). Pacientai taip pat vartojo ASS (nuo 75 mg iki 325 mg vieną kartą per parą).
Bet kurio tienopiridino vartojimas per 5 dienas iki registracijos buvo pašalinimo kriterijus. Kiti gydymo būdai, tokie kaip heparinas ir GPIIb / IIIa inhibitoriai, buvo skiriami gydytojo nuožiūra. Maždaug 40% pacientų (kiekvienoje gydymo grupėje) buvo gavę GPIIb / IIIa inhibitorių, skirtų palaikyti PKI (informacijos apie GP IIb tipą nėra). Maždaug 98% pacientų (kiekvienoje gydymo grupėje) buvo tiesiogiai gavę antitrombinų (heparino, mažos molekulinės masės heparino, bivalirudino ar kitų vaistų) kaip PKI.
Pagrindinis tyrimo rezultatų matas buvo laikas iki pirmojo širdies ir kraujagyslių (CV) mirties, nemirtino miokardo infarkto (MI) ar nemirtino insulto įvykio. Sudėtinė tikslo analizė visoje AKS populiacijoje (įskaitant UA / NSTEMI ir STEMI grupes) priklausė nuo statistinio prasugrelio pranašumo prieš klopidogrelį UA / NSTEMI grupėje įrodymo (p
Bendra AKS populiacija: Efient parodė didesnį veiksmingumą, palyginti su klopidogreliu, mažinant pirminę sudėtinę baigtį ir iš anksto nurodytas antrines baigtis, įskaitant stento trombozę (žr. 3 lentelę). Prasugrelio nauda buvo akivaizdi per pirmąsias 3 dienas ir tęsėsi iki tyrimo pabaigos. Didesnį veiksmingumą lydėjo padidėjęs kraujavimas (žr. 4.4 ir 4.8 skyrius). Pacientų populiacija buvo 92% baltaodžių, 26% moterų ir 39% vyresnių nei 65 metų. Naudos, susijusios su prasugreliu, nepriklausė nuo kitų ūminių ir ilgalaikių širdies ir kraujagyslių ligų gydymo būdų, įskaitant mažos molekulinės masės hepariną / hepariną, bivalirudiną, intraveninius GPIIb / IIIa inhibitorius, lipidų kiekį mažinančius vaistus, beta adrenoblokatorius ir angiotenziną konvertuojančio fermento inhibitorius. Prasugrelio veiksmingumas nepriklausė nuo ASR dozės (75-325 mg vieną kartą per parą). TRITON tyrimo metu nebuvo leidžiama vartoti geriamųjų antikoaguliantų, antitrombocitinių vaistinių preparatų, išskyrus tuos, kurie buvo tiriami, ir lėtinių NVNU. Visoje AKS populiacijoje prasugrelis buvo susijęs su mažesniu nemirtinų AMI mirčių dažniu ir nemirtino insulto, palyginti su klopidogreliu, neatsižvelgiant į pradines charakteristikas, tokias kaip amžius, lytis, kūno svoris, geografinis regionas, GPIIb / IIIa inhibitorių vartojimas ir stento tipas. Naudą daugiausia lėmė reikšmingas mirtingumo sumažėjimas AMI atvejai (žr. 3 lentelę) Diabetikai žymiai sumažino pirminius ir visus antrinius sudėtinius parametrus.
Prasugrelio nauda, pastebėta ≥ 75 metų pacientams, buvo mažesnė nei pacientams, sergantiems cukriniu diabetu, STEMI, padidėjusia stento trombozės ar pasikartojančių reiškinių rizika.
Pacientams, kuriems anksčiau buvo TIA arba buvo išemijos priepuolis, atsiradęs daugiau nei 3 mėnesius iki gydymo prasugreliu, pagrindinis tikslas nebuvo sumažintas.
3 lentelė. Pacientai, kurių klinikiniai rezultatai buvo atlikti atliekant pirminę TRITON tyrimo analizę
Visoje AKS populiacijoje kiekvienos antrinės baigties analizė parodė didelę naudą (p
Prasugrel buvo susijęs su stento trombozės sumažėjimu 50% per 15 mėnesių stebėjimo laikotarpį. Stentų trombozės sumažėjimas naudojant Efient buvo pastebėtas tiek metalo, tiek vaistinių stentų pradžioje ir po 30 dienų.
Analizuojant pacientus, išgyvenusius išeminį reiškinį, prasugrelis buvo susijęs su vėlesnių pirminių baigčių įvykių dažnio sumažėjimu (7,8% vartojant prasugrelį ir 11,9% vartojant klopidogrelį).
Nors kraujavimas padidėjo vartojant prasugrelį, sudėtinė „tikslo analizė“, kurią sudarė mirtis dėl visų priežasčių, nemirtinas miokardo infarktas, nemirtinas insultas ir su TIMI nesusijęs didelis kraujavimas, buvo palankus Efient, palyginti su klopidogreliu (HR 0,87) 95% PI, 0,79–0,95; p = 0,004). TRITON tyrimo metu kiekvienam 1000 Efient gydytų pacientų buvo 22 pacientai, sergantys miokardo infarktu, ir dar 5, kuriems buvo didelis su TIMI nesusijęs CABG kraujavimas, palyginti su pacientais, gydytais klopidogreliu.
Farmakodinamikos / farmakogenomikos tyrimo, kuriame dalyvavo 720 Azijos AKS sergančių pacientų, kuriems buvo atlikta PKI, rezultatai parodė, kad vartojant prasugrelį pasiekiamas didesnis trombocitų slopinimo lygis nei vartojant klopidogrelį ir kad 60 mg prasugrelio įkrovimo / 10 mg palaikomoji dozė yra tinkama dozavimo schema Azijos tiriamiesiems, kurie sveria ne mažiau kaip 60 kg ir yra jaunesni nei 75 metų (žr. 4.2 skyrių).
Per 30 mėnesių trukusį tyrimą (TRILOGY-ACS), atliktą 9326 mediciniškai gydytiems pacientams, sergantiems ACS UA / NSTEMI, be revaskuliarizacijos (neregistruota indikacija), prasugrelis reikšmingai nesumažino MI ar insulto mirties dažnio. Didelio kraujavimo (TIMI) dažnis (įskaitant mirties, mirtingumo ir intrakranijinio kraujavimo riziką) prasugreliu ir klopidogreliu gydytiems pacientams buvo panašus. ≥ 75 metų arba sveriantys mažiau nei 60 kg (N = 3022) atsitiktinės atrankos būdu sušvirkšta į 5 mg prasugrelio
05.2 Farmakokinetinės savybės
Prasugrelis yra provaistas ir greitai metabolizuojamas in vivo į aktyvų metabolitą ir neaktyvius metabolitus. Aktyvaus metabolito ekspozicija (AUC) skiriasi nuo vidutinio iki mažo (27%) ir atskirų asmenų (19%). Prasugrelio farmakokinetika yra panaši sveikiems asmenims, pacientams, kuriems yra stabili aterosklerozė, ir pacientams, kuriems atliekama perkutaninė vainikinių arterijų intervencija.
Absorbcija
Prasugrelio absorbcija ir metabolizmas yra greiti, o didžiausia aktyvaus metabolito koncentracija plazmoje (C aktyvus metabolitas nepakito riebiu ir kaloringu maistu, tačiau Cmax sumažėjo 49%, o laikas pasiekti Cmax (Tmax) padidėjo nuo 0, 5 iki 1,5 valandos. TRITON tyrimo metu Efient buvo skiriamas neatsižvelgiant į suvartojamą maistą, todėl Efient galima vartoti neatsižvelgiant į suvartojamą maistą; tačiau pavartojus pradinę prasugrelio dozę nevalgius, poveikis gali pasireikšti greičiau (žr. 4.2 skyrių).
Paskirstymas
Aktyvus metabolitas prisijungė prie žmogaus serumo albumino (4% buferinio tirpalo) 98%.
Metabolizmas
Išgerto prazugrelio plazmoje nėra. Žarnyne jis greitai hidrolizuojasi į tiolaktoną, kuris per vieną metabolizmo etapą citochromo P450, daugiausia CYP3A4 ir CYP2B6, ir mažesniu mastu - CYP2C9 ir CYP2C19, paverčiamas aktyviu metabolitu. Vėliau aktyvus metabolitas metabolizuojamas į du junginius neaktyvus dėl S-metilinimo arba konjugacijos su cisteinu.
Sveikiems asmenims, pacientams, kuriems buvo stabili aterosklerozė, ir pacientams, sergantiems AKS, kurie vartojo Efient, reikšmingo CYP3A5, CYP2B6, CYP2C9 arba CYP2C19 variacijos poveikio prasugrelio farmakokinetikai ar jos agregacijos slopinimui nebuvo.
Eliminavimas
Maždaug 68% prasugrelio dozės pašalinami su šlapimu ir 27% su išmatomis kaip neaktyvūs metabolitai. Aktyvaus metabolito pusinės eliminacijos laikas yra maždaug 7,4 valandos (nuo 2 iki 15 valandų).
Ypatingos populiacijos:
Vyresnio amžiaus piliečiai: Atliekant tyrimą su sveikais asmenimis nuo 20 iki 80 metų, amžius neturėjo reikšmingo poveikio prasugrelio farmakokinetikai ar jo gaminamo trombocitų agregacijos slopinimui. Didelio 3 fazės klinikinio tyrimo metu labai senyviems (≥ 75 metų amžiaus) pacientams aktyviojo metabolito (AUC) ekspozicija buvo 19% didesnė, palyginti su tiriamaisiais
Prasugrelį reikia vartoti atsargiai vyresniems kaip 75 metų pacientams, nes šioje grupėje gali atsirasti kraujavimo pavojus (žr. 4.2 ir 4.4 skyrius). Tyrimo su asmenimis, sergančiais stabilia ateroskleroze, vidutinė aktyvaus metabolito ekspozicija (AUC) ≥ 75 metų pacientams, vartojantiems 5 mg prasugrelio, buvo maždaug perpus mažesnė nei ≥ 75 metų pacientų.
Kepenų nepakankamumasPacientams, kuriems yra lengvas ar vidutinio sunkumo kepenų funkcijos sutrikimas (A ar B klasė pagal Child-Pugh), dozės koreguoti nereikia. Prasugrelio farmakokinetika ir trombocitų agregacijos slopinimas buvo panašūs tiriamiesiems, kuriems yra lengvas ar vidutinio sunkumo kepenų funkcijos sutrikimas, palyginti su sveikais. Prasugrelio farmakokinetika ir farmakodinamika pacientams, kuriems yra sunkus kepenų funkcijos sutrikimas, netirta. Jo negalima vartoti pacientams, kuriems yra sunkus kepenų funkcijos sutrikimas. sunkus kepenų funkcijos sutrikimas (žr. 4. 3 skyrių).
Inkstų nepakankamumas: Pacientams, sergantiems inkstų nepakankamumu, įskaitant pacientus, sergančius galutinės stadijos inkstų liga (ESRD), dozės koreguoti nereikia. Prasugrelio farmakokinetika ir trombocitų agregacijos slopinimas yra panašūs pacientams, kuriems yra vidutinio sunkumo inkstų funkcijos sutrikimas (glomerulų filtracijos greitis (GFR) 30-2) ir sveikiems asmenims. Prasugrelio sukeltos trombocitų agregacijos slopinimas buvo panašus. Taip pat pacientams, kuriems reikalinga hemodializė lyginant su sveikais tiriamaisiais, nors ESRD sergantiems pacientams aktyvaus metabolito Cmax ir AUC sumažėjo atitinkamai 51% ir 42%.
Kūno svoris: Aktyvių prasugrelio metabolitų ekspozicija (AUC) yra maždaug 30–40% didesnė sveikiems asmenims ir pacientams, kurių kūno svoris
Tautybė: Klinikinių farmakologijos tyrimų metu, pakoregavus kūno svorį, aktyvaus metabolito AUC kinų, japonų ir korėjiečių tiriamiesiems buvo maždaug 19% didesnis, palyginti su baltaodžiais, daugiausia dėl didesnės ekspozicijos Azijos tiriamiesiems, kurių kūno svoris
Seksas: Sveikų asmenų ir pacientų prasugrelio farmakokinetika moterims ir vyrams yra panaši.
Vaikų populiacija: Prasugrelio farmakokinetika ir farmakodinamika vaikų populiacijoje nebuvo įvertinta (žr. 4.2 skyrių).
05.3 Ikiklinikinių saugumo duomenys
Įprastų farmakologinio saugumo, kartotinių dozių toksiškumo, genotoksiškumo, galimo kancerogeninio poveikio ar toksiškumo reprodukcijai ikiklinikinių tyrimų duomenys ypatingo pavojaus žmogui nerodė. Poveikis ikiklinikinių tyrimų metu buvo pastebėtas tik esant ekspozicijai, kuri buvo pakankamai didelė didžiausia ekspozicija žmogui, o tai rodo mažą klinikinio naudojimo svarbą.
Toksikologiniai žiurkių ir triušių embriono ir vaisiaus vystymosi tyrimai neparodė prasugrelio sukeltų apsigimimų. Vartojant labai didelę dozę (> 240 kartų didesnę už rekomenduojamą palaikomąją žmogaus paros dozę mg / m2), kuri paveikė motinos kūno svorį ir (arba) maisto vartojimą, palikuonių kūno svoris šiek tiek sumažėjo (palyginti su kontroliniais) prieš ir po gimdymo tyrimų su žiurkėmis, gydymas motinomis neturėjo jokios įtakos palikuonių elgsenai ar reprodukcijai, skiriant dozes, iki 240 kartų viršijančias rekomenduojamą palaikomąją paros dozę (išreikštą mg / m2).
Dvejus metus trukusio žiurkių tyrimo metu nebuvo pastebėta su junginiais susijusių navikų, kurių prasugrelio ekspozicija buvo didesnė nei 75 kartus didesnė už rekomenduojamą terapinę ekspoziciją žmogui (remiantis aktyvaus metabolito ir žmogaus metabolitų ekspozicija žmogaus plazmoje. Pagrindiniai cirkuliacijoje). Pelėms, kurios dvejus metus buvo veikiamos didelėmis dozėmis (> 75 kartus didesnės už žmogaus ekspoziciją), „padidėjo navikų (kepenų ląstelių adenomų) dažnis, tačiau tai buvo laikoma antrine dėl prasugrelio sukelto fermento indukcijos. L“ Graužikams būdingas kepenų ryšys navikai ir vaistų sukelta fermentų indukcija yra gerai dokumentuota literatūroje. Kepenų navikų padidėjimas pelėms skiriant prasugrelį nelaikomas reikšminga rizika žmonėms.
06.0 FARMACINĖ INFORMACIJA
06.1 Pagalbinės medžiagos
Planšetės šerdis:
Mikrokristalinė celiuliozė
Manitolis (E421)
Kroskarmeliozės natrio druska
Hipromeliozė (E464)
Magnio stearatas
Dengimas:
Laktozės monohidratas
Hipromeliozė (E464)
Titano dioksidas (E171)
Triacetinas (E1518)
Raudonasis geležies oksidas (E172)
Geltonasis geležies oksidas (E172)
Talkas
6.2 Nesuderinamumas
Netaikoma.
06.2 Nesuderinamumas
2 metai.
06.3 Galiojimo laikas
2 metai.
06.4 Specialios laikymo sąlygos
Šiam vaistiniam preparatui specialios laikymo temperatūros nereikia. Laikyti gamintojo pakuotėje, kad vaistas būtų apsaugotas nuo oro ir drėgmės.
06.5 Pirminės pakuotės pobūdis ir pakuotės turinys
Aliuminio lizdinės plokštelės, supakuotos į 14, 28, 30, 30 (x1), 56, 84, 90 (x1) ir 98 tabletes.
Gali būti tiekiamos ne visų dydžių pakuotės.
06.6 Naudojimo ir naudojimo instrukcijos
Jokių specialių nurodymų.
07.0 RINKODAROS TEISĖS TURĖTOJAS
Eli Lilly Nederland BV, Grootslag 1-5, NL-3991 RA Houten, Nyderlandai.
08.0 RINKODAROS TEISĖS NUMERIS
EU/1/08/503/008
039055088
EU/1/08/503/009
039055090
EU/1/08/503/010
039055102
EU/1/08/503/011
039055114
EU/1/08/503/012
039055126
EU/1/08/503/013
039055138
EU/1/08/503/014
039055140
EU/1/08/503/016
09.0 RINKODAROS TEISĖS SUTEIKIMO AR PATVIRTINIMO DATA
Registravimo data: 2009 m. Vasario 25 d
Paskutinė atnaujinimo data:
10.0 TEKSTO PERŽIŪROS DATA
11.0 RADIJO NARKOTIKŲ VISIŠKAI VIDINIO RADIACIJOS Dozimetrijos duomenys
12.0 RADIJO NARKOTIKAI, PAPILDOMOS IŠSAMIOS NURODYMAI APIE LAIKINĄ PARUOŠIMĄ IR KOKYBĖS KONTROLĘ
SUSITARIA su EUROPOS MEDICINAL AGENCY (EMA) ir ITALIJOS Narkotikų agentūra (AIFA)
2013 m. Gruodžio mėn
Padidėjusi sunkaus kraujavimo rizika pacientams, sergantiems nestabilia krūtinės angina / ne ST segmento miokardo infarktu (UA) / NSTEMI, kai prieš diagnostinę koronarografiją skiriamas EFIENT (prasugrelis).
Gerbiamas daktare, gerbiamas daktare,
„Europos vaistų agentūra ir Italijos vaistų agentūra - AIFA, sutikusios su Daiichi -Sankyo ir Eli Lilly Italia, nori jus informuoti apie šią rekomendaciją dėl EFIENT (prasugrelio) - antitrombocitinio vaisto, skirto ūminiam ūmiam gydymui. koronarinis sindromas (AKS) pacientams, kuriems atliekama perkutaninė koronarinė intervencija (PKI):
Pacientams, sergantiems nestabiliąja krūtinės angina / miokardo infarktu (UA) / NSTEMI, kai koronarinė angiografija atliekama per 48 valandas po hospitalizavimo, įsotinamoji EFIENT dozė turi būti skiriama tik PCI metu, kad būtų sumažinta rizika nuo kraujavimo.
Ši rekomendacija yra pagrįsta neseniai atlikto klinikinio tyrimo su NSTEMI sergančiais pacientais, kuriems buvo atlikta koronarinė angiografija, rezultatais, praėjus 2–48 valandoms po atsitiktinės atrankos, rezultatais. Tyrime buvo lyginamas pradinės 30 mg prasugrelio pradinės įsotinamosios dozės prieš koronarinę angiografiją (vidutiniškai 4 val.), Po to „papildomos 30 mg dozės PKI metu“ ir poveikio, gauto vartojant vaistą, poveikis. pilna įsotinamoji 60 mg dozė PKI metu. Rezultatai parodė didesnę kraujavimo riziką, susijusią su pradinės įsotinamosios dozės vartojimu prieš koronarinę angiografiją, po to atlikus papildomą dozę PKI metu, palyginti su viena prisotinamąja prasugrelio doze PKI metu. pastebėtas tarp dviejų dozavimo režimų.
„ACCOAST“ tyrimas pavadintas: Prasugrel palyginimas poodinės koronarinės intervencijos metu arba kaip išankstinis gydymas diagnozės metu pacientams, sergantiems ne ST pakilusiu miokardo infarktu.
Sužinokite daugiau apie saugumo aspektus
ACCOAST buvo 30 dienų tyrimas, kuriame dalyvavo 4 033 pacientai, sergantys NSTEMI ir padidėjusiu troponinu, kuriems buvo atlikta koronarinė angiografija, o po to-2–48 valandos po atsitiktinės atrankos. Tiriamiesiems, kurie vidutiniškai likus 4 valandoms iki koronarinės angiografijos gavo 30 mg įsotinamąją prasugrelio dozę, po to 30 mg įsotinamąją dozę PKI metu (n = 2037), padidėjo kraujavimas tarp procedūrų, nesusijęs su CABG (nesusijęs) į vainikinių arterijų šuntavimo operaciją) ir jokios papildomos naudos pacientams, kuriems PKI metu buvo skirta 60 mg įsotinamoji dozė (n = 1996). Tiksliau tariant, tiriamiesiems reikšmingai nesumažėjo bendro tikslo-mirti nuo širdies ir kraujagyslių sistemos ligų, miokardo infarkto, insulto, skubios revaskuliarizacijos ar glikoproteino (GP) IIb / IIIa inhibitoriaus „panaudojant gelbėjimo terapiją“ dažnis per 7 dienas nuo atsitiktinės atrankos. vartoję prasugrelį prieš koronarinę angiografiją, palyginti su pacientais, kurie PK metu gavo visą prasugrelio įsotinamąją dozę. Be to, pagrindinio saugumo tikslo dažnis, išreikštas visu dideliu kraujavimu pagal TIMI (CABG ir ne CABG reiškiniai) per 7 dienas nuo atsitiktinės atrankos, visiems gydomiems asmenims, buvo žymiai didesnis tiriamiesiems, kurie gavo prasugrelį dviem dalimis (Likus 4 valandoms iki vainikinių arterijų angiografijos ir PKI), palyginti su pacientais, kuriems PK metu buvo skiriama visa pradinė prasugrelio dozė.
Pranešimas apie įtariamas nepageidaujamas reakcijas
Gydytojai ir kiti sveikatos priežiūros specialistai privalo pranešti apie bet kokias įtariamas nepageidaujamas reakcijas, susijusias su vaistais, kurių sudėtyje yra prasugrelio.
Gydytojai ir kiti sveikatos priežiūros specialistai pagal įstatymą privalo siųsti pranešimus apie įtariamas nepageidaujamas reakcijas, naudodami specialią popierinę formą (ją galima rasti svetainėje) http://www.agenziafarmaco.gov.it/sites/default/files/tipo_filecb84.pdf) arba nedelsdami užpildydami elektroninę formą internete (http://www.agenziafarmaco.gov.it/sites/default/files/scheda_aifa_oper_sanitario16.07.2 012.doc) sveikatos priežiūros įstaigos, kuriai jie priklauso, farmakologinio budrumo vadybininkui arba , jei ji veikia privačiose sveikatos priežiūros įstaigose, per Sveikatos departamentą - toje srityje kompetentingai ASL farmakologinio budrumo vadovei.
Tolimesnė informacija
Jei turite klausimų ir (arba) papildomos informacijos, kreipkitės į Eli Lilly „Medicinos informacijos“ biurą, skambindami šiuo nemokamu numeriu: 800117678 arba rašydami šiuo adresu: [email protected]
Pranešimai apie įtariamą nepageidaujamą reakciją iš vaistų turi būti siunčiami struktūros, kuriai priklauso operatorius, farmakologinio budrumo vadovui.
Ši informacinė pastaba taip pat skelbiama AIFA svetainėje (www.agenziafarmaco.it), kurioje rekomenduojama reguliariai konsultuotis, kad piliečiui būtų suteikta geriausia profesinė ir aptarnavimo informacija.